Wundinfektionen, die unter die Haut gehen
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
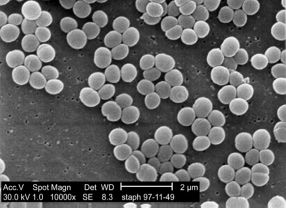
- Bakterien vom Typ Staphylococcus aureus sind häufig für schwere Wundinfektionen verantwortlich. Die Forscher im Verbundprojekt SkinStaph haben ihnen den Kampf angesagt. Quelle: Janice Carr / CDC
18.01.2011 -
Der Mikroorganismus Staphylococcus aureus zählt zu den häufigsten Erregern einer Infektion und kann in schweren Fällen zu einer lebensbedrohlichen Sepsis führen. Der Keim findet sich aber auch auf der Haut gesunder Menschen. Der Forschungsverbund „SkinStaph“ untersucht, wie sich die schweren Infektionen entwickeln und wie sie behandelt werden können. Das seit 2007 vom Bundesministerium für Bildung und Forschung (BMBF) geförderte Projekt wird vom Oberarzt Cord Sunderkötter an der Hautklinik des Universitätsklinikums Münster koordiniert.
Wegen des demographischen Wandels gibt es immer mehr ältere Menschen. Bei ihnen heilen Wunden häufig besonders schlecht und werden chronisch. Bakterien wie die Staphylokokken dienen diese Öffnungen als Einfallstor in den Körper, wo sie sich dann unter bestimmten Bedingungen unkontrolliert vermehren. Mit neuen Methoden versuchen die Wissenschaftler nun systematisch herauszufinden, wie genau die Infektion des Weichgewebes gelingt. Denn noch ist unklar, wieso es häufig bei der bloßen Besiedlung von Wunden bleibt und wann es zur Infektionen des Gewebes kommt.
| Mehr auf biotechnologie.de |
Förderbeispiel: Mit Antikörpern gegen multiresistente Bakterien News: Wie ein neues Antibiotikum gegen multiresistente Bakterien wirkt Menschen: Dirk Bumann - Macht gefährlichen Bakterien den Garaus |
„Möglicherweise liegt das an der Virulenz des Erregers, also sozusagen seiner Gefährlichkeit. Oder es spielen hauptsächlich sogenannte Wirtsfaktoren eine Rolle, beispielsweise Unterschiede im Immunsystem der Betroffenen“, erklärt Sunderkötter. Wie groß der Einfluss dieser beiden Mechanismen ist, das will er gemeinsam mit Kollegen von den Universitäten in Bonn, Tübingen, Saarbrücken, Gießen und Kiel sowie dem Helmholtz-Zentrum für Infektionsforschung in Braunschweig herausfinden. „Wir suchen nach den Ursachen und neuen Therapiemöglichkeiten von Haut- und Weichgewebeinfektionen durch Staphylokokken“, sagt Sunderkötter.
Erreger sind häufig Antibiotika-resistent
Denn bisher gestaltet sich die Behandlung dieser Infektionen häufig schwierig: „Angesichts des Aufkommens hochresistenter Bakterienstämme sind neue Konzepte zur Prävention und Kontrolle erforderlich“, so der Dermatologe Sunderkötter. Die Gefahr, die von Staphylococcus aureus ausgeht, ist nicht zu unterschätzen: Gelangen die Bakterien ins Blut, kann es zur Sepsis, zur Blutvergiftung, kommen. Mediziner fürchten schwere Verläufe dieser Erkrankung, die trotz einer Maximaltherapie in 30 bis 50 Prozent aller Fälle mit dem Tod des Patienten enden.
Die Forscher, die bei ihrer Arbeit vom BMBF unterstützt werden, untersuchen schon seit 2007 die verschiedenen Schritte der Infektion. „Einer der Höhepunkte der bisherigen Forschungsarbeit ist zum Beispiel die Erkenntnis, dass bestimmte antimikrobielle Eiweiße der Haut, die Defensine, die Bakterienwand nicht nur schwächen, sondern in der Lage sind, ihre Synthese zu verhindern“, so Sunderkötter. Offenbar wirken sie ähnlich wie klassische Antibiotika. Sie stören den Aufbau der Zellwand, indem sie mit einigen ihrer Moleküle reagieren, so dass nicht zu stopfende Löcher in der Wand entstehen. Entdeckt wurde das erst im Juni durch am Verbundprojekt beteiligte Forscher um Georg Sahl aus Bonn (mehr…).
In Münster konzentrieren sich die Forscher auf eine andere Fragestellung. Sie vergleichen die Bakterien
aus Patientenproben miteinander. Sind die Mikroben, die sich auf der Haut finden lassen identisch mit
SkinStaph |
Im SkinStaph-Netzwerk untersuchen Forscher die einzelnen Schritte einer Infektion mit Staphylococcus aureus. Das Projekt wird vom Bundesministerium für Bildung und Forschung gefördert. Zum Verbundprojekt SkinStaph auf den Seiten des BMBF: hier klicken Zur Homepage des SkinStaph-Netzwerkes: hier klicken Zur Homepage der Hautklinik am Universitätsklinikum Münster: hier klicken |
denen aus infizierten Wunden? Gleichen ihnen auch die Bakterien aus den tiefen Weichteilinfektionen? „Die Ergebnisse aus einer Gewebebank des Netzwerkes weisen darauf hin, dass chronische Wunden zwar von vielen Bakterien besiedelt werden, aber dass nur ganz bestimmte Bakterien unter ihnen eine Infektion im Gewebe verursachen“, so Sunderkötter. Auf sie ließe sich künftig Prophylaxe und Behandlung konzentrieren, glaubt der Mediziner.
Gerade dieses Projekt ist auch für den klinischen Alltag von besonderer Bedeutung: Nur wenn sich klären lässt, welche Bakterien tatsächlich für die Entzündung verantwortlich sind, kann auch das passende Antibiotikum gewählt werden. Die Patienten könnten dann von einer Therapie profitieren, die nicht nur weniger kostet, sondern auch mit geringeren Nebenwirkungen verbunden ist. Auf Basis der bisherigen Erfolge hat das BMBF einer weiteren Förderung bis 2013 zugestimmt und stellt dafür 2,2 Mio. Euro zur Verfügung.