Carsten Watzl: Mit Natürlichen Killerzellen gegen Krebs
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
- Carsten Watzl ist Immunologe an der Universität Heidelberg. Quelle: Watzl
27.08.2008 -
Natürliche Killerzellen gehören zur schnellen Eingreiftruppe im angeborenen Immunsystem des Menschen. Sie töten krankhaft veränderte und körperfremde Zellen und sind – anders als die meisten anderen Immunzellen – ohne vorherige Stimulation einsatzfähig. Carsten Watzl beschäftigt sich damit, wie diese Zellen eigentlich zwischen Freund und Feind unterscheiden können. Für den Professor am Institut für Immunologie der Universität Heidelberg sind die kleinen Zerstörer unter anderem deshalb interessant, weil sie Krebszellen erkennen – besonders gegen Blutkrebs können sie viel ausrichten. Der 37jährige hat sich zum Ziel gesetzt, die Aktivität der Killerzellen künstlich zu initiieren und diesen Ansatz als Krebstherapie zu nutzen. Seit 2005 wird er dabei mit dem BioFuture-Preis des Bundesministeriums für Bildung und Forschung (BMBF) unterstützt.
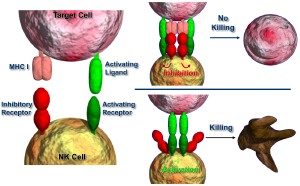
Natürliche Killerzellen (NK-Zellen) sind eine Untergruppe der weißen Blutkörperchen (Lymphozyten) und gehören zum angeborenen Immunsystem. Sie befinden sich in Blut, Lymphe sowie Organen und reagieren am schnellsten auf Krankheiten und Eindringlinge im Körper. „Minuten bis Stunden nach einer Infektion werden die Jungs aktiv“ erklärt Watzl. Der Immunologie-Professor an der Universität Heidelberg setzt sich schon seit Jahren mit der Frage auseinander, woher die angeborenen Zerstörer eigenlich wissen, wen sie angreifen dürfen und wen nicht. Inzwischen ist bekannt, dass Antennen auf der Oberfläche der evolutionär sehr alten Killerzellen dabei eine entscheidende Rolle spielen. Diese Antennen, auch Rezeptoren genannt, haben aktivierende und hemmende Funktionen. Erstere dienen zur Erkennung von Molekülen auf anderen Zellen, letztere sind für einen bestimmten Eiweißkomplex zuständig. Dieser wird von Immunologen MHC-1 genannt, der bei fast jeder körpereigenen Zelle auf der Oberfläche vorkommt. „Er ist wie ein Ausweis“, so Watzl.
Ausweis verhindert Angriff auf eigene Zellen
Für die Killerzellen ist er enorm wichtig: Erkennen sie diesen Ausweis, senden sie ein negatives Signal ins Innere und werden damit ausgeschaltet. Nur auf diese Weise bleibt sichergestellt, dass gesunde Körperzellen nicht angegriffen werden. Anders sieht es hingegen bei Tumorzellen oder infizierten Körperzellen aus. Sie verlieren den MHC-1-Komplex häufig und werden damit zum Zielobjekt der natürlichen Zerstörer. „Das Fernziel ist, die NK-Zellaktivität zu beeinflussen und ihre Wirkung – etwa gegen Krebs – dadurch zu unterstützen“, so Watzl. So könnten Spender für die Knochenmarkstransplantion von Leukämie-Patienten so ausgewählt werden, dass die Natürlichen Killerzellen der Spender die Krebszellen der Patienten gezielt bekämpfen. Andere Ansätze zielen darauf ab, die Natürlichen Killerzellen außerhalb des Körpers zu vermehren, zu aktivieren und anschließend dem Krebspatienten wieder zu injizieren – um auf diese Weise, gut gerüstet gegen die Krankheit vorgehen zu können. Wieder andere Strategien sehen vor, die körpereigenen Natürlichen Killerzellen so zu stärken, dass sie die Krebszellen effektiv angreifen und abtöten können.
Watzl: Noch bestehende Wissenslücken klären
Noch allerdings haben die Forscher noch etliche Wissenslücken und Watzl gehört zu denjenigen, die weitere Details auf molekularer Ebene klären wollen. Zum Beispiel, wie die Natürlichen Killerzellen aktivierende und hemmende Signale verrechnen. Denn „normalerweise kriegen sie ständig ein bißchen was von beiden“, erklärt der Forscher. Die Reaktion der Killerzellen richtet sich also nach einer feinen Balance zwischen diesen beiden Signalen. Ganz verstanden ist diese Regulation bis heute nicht, aber Watzl konnte immerhin herausfinden, dass sogenannte Lipid Rafts eine entscheidende Rolle spielen.
| BioFuture-Wettbewerb |
Watzl ist einer 51 Preisträgern, die sich im BioFuture-Wettbewerb des Bundesministeriums für Bildung und Forschung (BMBF) durchgesetzt haben. biotechnologie.de hat bereits andere BioFuture-Gewinner porträtiert: Henning Walczak: Das Selbstmordprogramm der Zelle im Visier Marcus Fändrich: Von Fibrillen und Prognosen Ute Krämer: Den Mechanismen pflanzlicher Metallfresser auf der Spur Erich Wanker: Will Chorea Huntington auf den Pelz rücken |
Dabei handelt es sich um bestimmte Areale in der Hülle der Zelle, die sich von ihrer Umgebung wie eine kleine Insel durch ihre Fettsäure- und Eiweißzusammensetzung unterscheiden. „Wenn die aktivierenden Rezeptoren stimuliert werden, gehen sie in diese Lipid Rafts rein“, erläutert Watzl. „Und sie brauchen sie auch für ihre Funktion, denn wenn man sie entfernt, können die Rezeptoren die NK-Zellen nicht mehr richtig anschalten“ erzählt er weiter. Warum das so ist, kann auch Watzl noch nicht sagen. Er weiß nur, dass diese Tatsache von den hemmenden Rezeptoren genutzt wird. Sind diese erstmal angeregt, können die aktivierenden Rezeptoren nicht mehr in das Areal der Lipid Rafts einwandern – und ergo ihre schützende Zerstörerkraft gegen Eindringlinge nicht ausüben.
Forschung mit Umwegen
Um diese komplexen Zusammenhänge noch besser zu verstehen, wollte Watzl eigentlich alle Faktoren in den Lipid Rafts untersuchen und so herausfinden, welche sich ändern, wenn die Zelle aktiv oder inaktiv ist. „Da sind wir in technische Probleme gelaufen“, so Watzl über die Versuche und weiter: „Wir mussten komplett neue Methoden entwickeln, um diese Eiweiße überhaupt zu isolieren“. Das hat den Forscher zwei Jahre zurückgeworfen. Jetzt allerdings stehen die Methoden und Watzl ist guter Hoffnung, bald ein paar aussichtsreiche Kandidaten zu finden.
| Mehr zum Thema auf biotechnologie.de |
Dossier: Biotechnologie und Krebs |
Eigentlich kommt Watzl aus einer anderen Ecke der Wissenschaft – der Erforschung des natürlichen Selbstmordprogramms von Zellen, der Apoptose. Für Natürliche Killerzellen interessiert er sich erst nach der Promotion am Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg. „Zu der Zeit wurden gerade diese hemmenden Rezeptoren der NK-Zellen identifiziert“ erinnert sich der Forscher. Die Sache war völlig neu und unverstanden. „Ich dachte, da kann man noch was machen“, erzählt er. Dreieinhalb Jahre forscht Watzl als Postdoktorand in der Gruppe von Dr. Eric O. Long am National Institute of Allergy and Infectious Diseases (NIAID), National Institutes of Health, Rockville, MD, USA, und legt dort den Grundstein für seine heutige Forschung. „Das NIH ist ein riesengroßer Campus, da trifft man die Topleute fast täglich. Das gibt es so in Deutschland nicht“, sagt Watzl.
Als Forscher in Deutschland gut aufgehoben
Dass die Wissenschaftslandschaft in Deutschland schlechter ist, bestreitet er jedoch. So entscheidet sich der Deutsche nach seinem Postdoc auch wieder für eine Rückkehr in die Heimat – wegen der besseren Förderung. Mithilfe einer fünfjährigen Nachwuchsförderung in einem Sonderforschungsbereich (SFB) der Deutschen Forschungsgemeinschaft an der Universität Heidelberg baut sich Watzl seine eigene Arbeitsgruppe auf: „Von Stellenausstattung und Zeitrahmen ist das etwas, was man in den USA nicht findet“. Im Jahr 2005 setzt er sich zudem beim BioFuture-Wettbewerb des Bundesministeriums für Bildung und Forschung (BMBF) durch. Für fünf Jahre erhält er dadurch ein Forschungsbudget von rund einer Millionen Euro.
Im Augenblick kann sich Watzl ein Leben ohne Wissenschaft nicht vorstellen: „Ich habe da mein Hobby zum Beruf gemacht.“ Wichtig ist ihm dabei vor allem eines; die persönliche Freiheit. „Ich kann beforschen, was mir Spaß macht. Das würde ich in einer Firma nicht finden“ sagt er. Einziger Wermutstropfen: Im Labor stehen, dafür ist leider keine Zeit mehr.
Autorin: Miriam Ruhenstroth