Alzheimer: Molekularer Schneeballeffekt lässt Proteine verklumpen
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
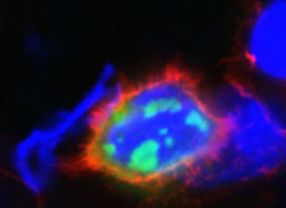
- Giftige Proteinklumpen (grün) führen in menschlichen Zellen dazu, dass sie absterben. Die Aggregate sind eine Ursache für Hirnleiden wie Alzheimer oder Parkinson. Quelle: Heide Olzscha/Max-Planck-Institut für Biochemie
12.01.2011 -
Giftige Proteinklumpen in Nervenzellen gelten als eine Ursache für das zelluläre Massensterben, wie es in den Gehirnen von Alzheimer- oder Parkinson-Patienten passiert. Wissenschaftler am Max-Planck-Institut für Biochemie in Martinsried bei München haben aufgeklärt, wie in der Zelle giftige Proteinaggregate entstehen und welche Proteine dafür anfällig sind. Wie die Forscher im Fachjournal Cell (7. Januar 2010, Bd. 144, S. 67) berichten, haben sie mithilfe von künstlichen Proteinen in menschlichen Zellen Verklumpungsreaktionen in Gang gesetzt. Die Protein-Aggregate wuchsen heran und zogen dabei wie bei einer molekularen Lawine immer mehr andere Eiweiße in Mitleidenschaft. Molekulare Chaperone könnten nach Ansicht der Forscher dabei helfen, dass schädliche Eiweißklumpen gar nicht erst entstehen.
Um ihre verschiedenen Funktionen im Körper wahrnehmen zu können, müssen Proteine korrekt gefaltet sein und die richtige dreidimensionale Struktur besitzen. Dafür sorgen Chaperone, die „molekularen Anstandsdamen“ der Zelle. Erfüllen sie ihre Aufgabe nicht, sind Fehlfaltungen oder ein Verklumpen der Proteine die Folge. Das kann wiederum zu neurodegenerativen Erkrankungen wie Alzheimer, Huntington oder Parkinson führen. Alzheimer etwa entsteht, weil die entstandenen Proteinaggregate toxisch auf Nervenzellen wirken und diese absterben lassen. Nach Angaben von Alzheimer Forschung Initiative e.V. leiden in Deutschland schätzungsweise 1,2 Millionen Menschen an dieser Krankheit, wobei das Risiko mit steigendem Alter zunimmt.
Die Klumpenbildung künstlich ausgelöst
Wissenschaftler der Abteilung Zelluläre Biochemie am Max-Planck-Institut für Biochemie, die von Ulrich Hartl (mehr zu seinem Profil: hier klicken) geleitet wird, haben jetzt herausgefunden, wie Proteine zu Aggregaten verklumpen und warum das für Zellen schädlich ist. Dazu haben sie zunächst künstliche Proteine ohne jegliche biologische Funktion hergestellt und in menschliche Zellen eingeschleust.
| Mehr auf biotechnologie.de |
News: Schutzengel für Eiweiße in 3D nachgebaut News: Nachschub bei Alzheimer - Gehirn bildet neue Nervenzellen Menschen: Franz-Ulrich Hartl: Die Rolle der Anstandsdame unter den Eiweißen aufgeklärt |
Die Kunstproteine lagerten sich in den Zellen zu Klumpen zusammen. Dieser Vorgang entwickelte dann aber eine fatale Eigendynamik: Die Klumpen zogen viele natürliche Proteine der Zelle in die Aggregate hinein und störten so deren Funktion. Mithilfe von Messverfahren der Proteomik konnten die Wissenschaftler zudem herausfinden, dass die betroffenen Eiweißmoleküle bestimmte strukturelle Eigenschaften gemeinsam haben, die eine Aggregation erst ermöglichen: Sie sind groß, besitzen mehrere Funktionsbereiche und weisen eine erhebliche, ungeordnete Struktur auf.
„Hierbei handelt es sich um Proteine, die nicht nur viele, sondern vor allem äußerst wichtige Funktionen in der Zelle erfüllen“, erklärt Max-Planck-Forscher Martin Vabulas.
Chaperone könnten den zellulärer Systemabsturz verhindern
Die in Mitleidenschaft gezogenen Proteine seien beispielsweise für die Organisation und Stabilität innerhalb der Zelle, die Umwandlung von DNA in RNA oder die Herstellung von Proteinen verantwortlich. Vabulas: „Werden mehrere dieser essentiellen zellulären Funktionen gleichzeitig gestört, führt das zum zellulären Systemabsturz. Krankheiten wie Alzheimer, Huntington oder Parkinson sind die Folge.“
Die Martinsrieder Biochemiker haben auch schon Ideen, wie sich die Entstehung der giftigen Eiweißklumpen stoppen ließe. Demnach könnte eine erhöhte Bildung bestimmter Chaperone die Proteinaggregationen verhindern oder abbremsen. Denn die Chaperone schirmen die Aggregate ab, sodass sie nicht mehr mit anderen Proteinen in Kontakt treten können. Nach Ansicht der Forscher könnte dies ein möglicher Ansatzpunkt im Kampf gegen neurodegenerative Krankheiten sein. So ließe sich womöglich Alzheimer, Huntington oder Parkinson schon verhindern, bevor die Leiden entstehen.