Paul Saftig: Die Alzheimer-Scheren stumpfer machen
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
- Paul Saftig ist einer der drei Direktoren des Instituts für Biochemie der Universität Kiel. Quelle: Andrea Dankwardt
01.02.2011 -
Noch ist der Entstehungsmechanismus von Alzheimer nicht restlos geklärt. Eine verheerende Rolle spielen auf jeden Fall kleine Eiweißschnipsel, die sich im Gehirn ansammeln und zu sogenannten Plaques verklumpen. Die umliegenden Nerven sterben ab, die kognitiven Fähigkeiten sinken. Paul Saftig von der Universität Kiel interessiert sich für die molekularen Scheren, die die Eiweißschnipsel produzieren. In den vergangenen zwölf Jahren untersuchte der Biologe im Besonderen drei Gene, die für die Bildung derartiger Alzheimer-Scheren verantwortlich sind. Überraschenderweise haben die Scheren, die bei Alzheimer-Patienten so viel Schaden anrichten, offenbar auch eine nützliche Rolle. Für diese Entdeckung bekam Saftig jetzt den höchsdotierten Alzheimerpreis Deutschlands verliehen.
Manchmal sind es gemeinsame Kneipenabende, die einen jungen Forscher auf neue Ideen bringen. Paul Saftig hatte seine Promotion gerade abgeschlossen, als er Mitte der 90er Jahre Gastforscher an der belgischen Universität Leuven war. Beim abendlichen Gespräch mit Forscherkollegen kam die Rede auf Presenilin 1 und 2, Bezeichnungen für zwei Gene im menschlichen Erbgut. Den belgischen Kollegen war aufgefallen, dass Patienten mit einer Mutation dieser Gene unter besonders schwer verlaufenden Formen von Alzheimer litten. Als Spezialist für Experimente mit so genannten Knockout-Mäusen schlug Paul Saftig kurzerhand eine Kooperation vor, um die biologische Funktion von Presenilin 1 und 2 zu klären. Wenig später fand er zusammen mit dem belgischen Team heraus, dass eines der beiden Gene bei der Bildung von Alzheimer-Scheren verantwortlich ist.
| Weiße Biotechnologie |
News: Alzheimer - Molekularer Schneeballeffekt lässt Proteine verklumpen Förderbeispiel: Modelle simulieren Alzheimer-Stoffwechsel Menschen: Katharina Zimmermann - Alzheimer-Expertin aus der Industrie an die Hochschule |
Knockout-Mäuse liefern mögliche Therapieansätze
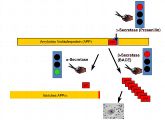
Die gefürchteten Eiweißablagerungen im Gehirn der Betroffenen bestehen zum größten Teil aus beta-Amyloid. Das ist ein kleines Eiweißmolekül, das entsteht, wenn bestimmte Enzyme, die Alzheimer-Scheren, ein größeres Eiweiß in der Nervenzelle zerschneiden. In Kooperation mit den belgischen Forschern züchtete Saftig Knockout-Mäuse, bei denen das Gen Presenilin 1 ausgeschaltet war. In den Nervenzellen dieser Mäuse war die Produktion des beta-Amyloid im Vergleich zu Nervenzellen von Kontrollmäusen um 80 Prozent reduziert und die Forscher schlussfolgerten, dass sie durch Hemmung des Gens Presenilin 1 die Bildung und Ablagerung der Plaques verringern können.

Nach diesem ersten großen Forschungserfolg habilitierte Paul Saftig sich in Göttingen und wurde 2001 als Professor und einer der drei Direktoren des Biochemischen Instituts an die Universität Kiel berufen. Aus seiner Zeit in Belgien nahm der in Hennef geborene Biologe das Bewusstsein eines europäischen Forschungsraums mit. In seinen Forschungsprojekten kollaboriert er mit Universitäten aus ganz Europa. „Diese Kooperationen mit anderen Forschergruppen sind enorm wichtig, um voran zu kommen“, erklärt er.
Krank machende Enzyme haben wichtige Funktionen
Saftig ist seinem Forschungsthema treu geblieben. Inzwischen hat sein Team weitere Gene erforscht, die für bestimmte Alzheimer-Scheren verantwortlich sind. Das Entscheidende dabei: „Alle spaltenden Eiweiße haben mehrere Funktionen, die es zu erforschen gilt, wenn man einer Therapie näher kommen will“, erklärt der 48-Jährige. So ist die beta-Sekretase, kurz BACE, einerseits als Scherenenzym ein möglicher Auslöser für die Alzheimersche Krankheit, andererseits aber auch wichtig für die gesunde Nervenfunktion des Körpers.
Für seine Arbeiter erhielt Saftig den mit 100.000 € ausgezeichneten Hans und Ilse Breuer Preis für Alzheimerforschung 2011. Die Auszeichnung wurde zum sechsten Mal in Folge verliehen und ist die höchstdotierte Auszeichnung für Alzheimerforschung in Deutschland.
| Hintergrund |
Sie wollen sich intensiver über die Arbeiten von Paul Saftig informieren? Dann besuchen Sie den Webauftritt der Abteilung für Zellbiologie und transgenische forschung des Instituts für Biochemie der Universität Kiel. zur Abteilung Saftig: hier klicken |
Das Enzym schneidet aus dem Vorläuferprotein das beta-Amyloid heraus, welches zu Plaques verklumpt, ist aber auch für die Myelinisierung von Nervenzellen notwendig. Dabei wickeln sich Gliazellen um die Neuronen und ermöglichen unter anderem die rasche Signalweiterleitung am Nerv. „Unser langfristiges Ziel ist es nun, das richtige therapeutische Fenster zu finden. Wir wollen die Enzyme etwas blocken, dabei aber die Nebenwirkungen möglichst gering halten“, so Saftig. Denn die nützlichen Funktionen der Enzyme sollen beibehalten werden.
Bis zu einer Therapie ist es zumeist ein weiter Weg, aber die Forscher haben gelernt, langfristig zu denken. So prüft Saftig derzeit Erkenntnisse, die noch ganz vom Beginn seiner Karriere stammen.In einer klinischen Studie wird derzeit ein Medikament gegen die seltene Erbkrankheit α-Mannosidose getestet. Auch hier spielen Enzyme eine Rolle, deren Substrate sich übermäßig im Gewebe der Betroffenen anreichern. Im Mausmodell hatte das Team um Saftig herausgefunden, dass eine mehrmalige Gabe des fehlenden Enzyms das Krankheitsbild dramatisch verbessert. „Das ist im Grunde noch ein Ergebnis meiner Forschung aus meiner Doktorarbeit, und wir freuen uns, dass diese Erkenntnisse nun auch in die Behandlung von Patienten einfließen“, meint er. Das kann nicht jeder Grundlagenforscher von sich behaupten.
Autorin: Ute Zauft