Regenerative Medizin: Knorpel zum Nachwachsen angeregt
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
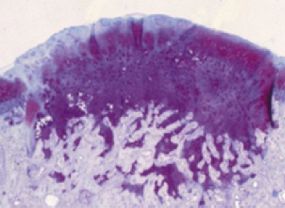
- Mit dem nachgezüchtetem Knorpelgewebe (dunkelviolett) lassen sich großflächige Gelenknorpel-Defekte heilen. Quelle: Prasad Shastri/PNAS
16.02.2010 -
Fast jeder Dritte Erwachsene in Deutschland leidet an einer Arthrose, also einer fortschreitenden Verschleißerkrankung an mindestens einem Gelenk. Gewöhnlich wird eine Arthrose mithilfe von Schmerzmitteln gelindert, als letzte Rettung gelten oftmals Prothesen. Regenerative Therapien zielen dagegen darauf ab, abgenutzte Gewebe auf biotechnologischem Wege wieder aufzubauen. Bei Knorpel gelingt das schon vergleichsweise gut, doch bislang können damit nur kleine verletzte Bereiche behandelt werden. Zudem ist die Prozedur der Knorpelzüchtung sehr aufwendig und teuer. Forscher um den Gewebe-Experten Prasad Shastri vom Zentrum für Biologische Signalstudien BIOSS der Universität Freiburg berichten jetzt im Fachblatt PNAS (Online-Vorabveröffentlichung, 4. Februar 2010) von einem deutlich verfeinerten Verfahren: Darin wird der Körper selbst zum Knorpel-Fabrikanten.
Während Knochengewebe dank im Knochenmark vorkommender Stammzellen eine erstaunliche Regenerationskraft besitzt, sieht das bei Knorpelgewebe anders aus. Knorpel erneuert sich im Körper kaum. Gerade in den Gelenken nutzt sich der Knorpel im Laufe des Lebens ab, er wird spröde und anfällig für Verletzungen, wie etwa der Meniskus oder die Bandscheiben. Knorpel besteht allerdings auch aus nur einem einzigen Zelltyp, den Chondrozyten. Deshalb ist er ein aussichtsreicher Kandidat für die Gewebenachzüchtung im Labor.
| BIOSS |
Das Zentrum für biologische Signalstudien (bioss) benutzt Methoden der Synthetischen Biologie, um die komplexen Abläufe biologischer Signalprozesse zu verstehen und vielleicht einmal zu steuern. Zur Website des BIOSS: hier klicken |
Inzwischen ist die Kunst der künstlichen Knorpelherstellung schon relativ weit entwickelt, einige Anwendungen werden bereits in der Praxis genutzt, andere werden noch in klinischen Studien erprobt. Gerade hier zeigt sich die neue Ausrichtung der Medizin weg von der Reparatur mit Prothesen hin zur Regeneration mit im Labor hergestellten Zell-Gewebe-Konstrukten. Im Idealfall sollen diese Implantate vorübergehend durch Freisetzen von Wachstumsfaktoren die körpereigenen Regenerationskräfte ankurbeln. Dazu nutzen die Gewebe-Ingenieure verschiedene Mixturen aus Biomaterialien, Signalmolekülen und Zellen.
Bisher nur kleine Knorpelschäden heilbar
Lange Zeit galt Knorpel als nicht heilbares Gewebe, der künstliche Gelenkersatz mit Prothesen blieb die einzige Wahl für die Ärzte. Erst seit Mitte der 1990er Jahre wurde eine Technik entwickelt, um lokale Knorpeldefekte, wie sie nach Verletzungen entstehen, mithilfe von biokünstlichen Transplantaten zu kurieren, die aus Knorpelzellen der Patienten herangezüchtet werden. Pro Jahr werden in Deutschland mittlerweile etwa 2000 Betroffene mit einer solchen Autologen Chrondrozyten-Transplantation (ACT) behandelt. Einem Patienten werden dazu aus dem Knie winzige Knorpelproben entnommen, aus denen die Chondrozyten isoliert werden. Während die Zellen im Körper recht träge sind, lassen sie sich in der Kulturschale inzwischen ganz gut vermehren. Auf einer Stützunterlage können sie zu neuem Gewebe herangezüchtet werden. Allerdings sind diese Verfahren sehr aufwendig: die Zellen des Patienten müssen isoliert, aufgereinigt, vermehrt und zu funktionsfähigem Gewebe gezüchtet werden. Bislang können mit der ACT nur kleine lokale Defekte passgenau ausgebessert werden. Oft ist unklar, wie gut sich die Implantate in die betroffenen Stellen einfügen und wie sie auf jahrelange Belastung reagieren. Noch nicht geeignet ist das Verfahren für die hunderttausenden Patienten, die unter Gelenkverschleiß leiden, zum Beispiel am Knie.
| Mehr zum Thema auf biotechnologie.de |
News: Regenerative Medizin: Salamander offenbart völlig neue Erkenntnisse |
Sauerstoffmangel lässt die Knorpelzellen sprießen
Der Forscher Prasad Shastri ist ein Experte für die Gewebekonstruktion und Gewebezüchtung aus körpereigenen Zellen (Tissue Engineering). Der gebürtige Inder arbeitete als Postdoc bei Gewebezucht-Pionier Robert Langer am MIT in Boston und zuletzt an der Vanderbuilt University in Nashville. Vor einem Jahr gelang es der Freiburger Universität, den renommierten Forscher aus den USA nach Deutschland als Professor für Biofunktionale Makromolekulare Chemie ans Zentrum für Biologische Signalstudien (BIOSS) zu holen. Nun hat er gemeinsam mit Kollegen aus dem niederländischen Maastricht ein Verfahren entwickelt, mit dem sich langfristig womöglich auch größere Knorpeldefekte reparieren lassen. Wie die Forscher im Fachmagazin PNAS (Online Vorabveröffentlichung, 4, Februar 2010) berichten, haben sie es geschafft, an bestimmten Körperstellen lebender Kaninchen umfangreiches Wachstum von neuem Knorpelgewebe auszulösen.
Viele bisherige Gewebezüchtungs-Ansätze setzen auf Knorpelzellen, die dem Patienten entnommen und außerhalb des Körpers in Wachstumskammern, so genannten Bioreaktoren, herangezüchtet werden. Die Freiburger hingegen verfolgten ein in vivo-Verfahren: Neuer Knorpel soll im Patienten selbst herangezüchtet werden, der Körper wird hierbei selbst zum Bioreaktor. Der Trick: Die Forscher spritzten bei Kaninchen zunächst ein Agarose-Gel unter die Knochenhaut des Schienbeins. Agarose ist eine gängige Laborchemikalie, die gewöhnlich zu einer gallertartigen Masse verrührt wird, um damit etwa Erbgutfragmente aufzutrennen. Bei der Knorpelzüchtung im lebenden Gewebe sorgt das Agarose-Gel nun offenbar für einen lokalen Sauerstoffmangel, der wiederum die umfangreiche Bildung von hyalinem Knorpel unter der Knochenhaut stimuliert. "Das ist die erste Arbeit, die die Knorpelzüchtung im lebenden Körper zeigt", betont Prasad Shastri.
Der Patient als Knorpel-Bioreaktor
Die Forscher entnahmen daraufhin den gezüchteten Knorpel und setzten sie bei denselben Tieren in einen defekten Gelenkknorpel ein. "Die nachgezüchteten Implantate fügten sich gut in den Defekt ein und waren auch nach neun Monaten noch nicht verkalkt", sagt Shastri. Wie der durch Agarose ausgelöste Prozess auf molekularer Ebene abläuft, ist noch nicht verstanden - dies wollen die Forscher als Nächstes aufklären. Aus ihrer Sicht hat ihr Verfahren jedoch den Vorteil, dass keine Wachstumsfaktoren eingesetzt werden müssen, die bei einer späteren Zulassung für eine medizinische Anwendung einen größeren Aufwand bereiten. Aus diesem Grund halten die Forscher ihre Strategie für eine interessante Alternative künftiger regenerativer Knorpel-Therapien. "Innerhalb der nächsten zwei Jahre wollen wir mit Pilotstudien für das Verfahren bei geeigneten Patienten beginnen", so Shastri. Hier soll zunächst getestet werden, wie sicher die Knorpel-Nachzüchtung im Schienbein ist.