Wochenrückblick KW 50
Rückblick auf Kalenderwoche 50
Für den Zeitraum vom 9. bis 16. Dezember 2013 hat biotechnologie.de für Sie die wichtigsten Nachrichten aus der Biotech-Branche zusammengestellt.
Neue Regierungsposten: Von Forschung bis Entwicklung
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
- Johanna Wanka bleibt auch weiterhin Bundesministerin für Bildung und Forschung. Der bisherige Innenminister Hans-Peter Friedrich (CSU) leitet künftig das Agrarressort. Quelle: Axel Hindemith/wikipedia.org/CC-by-sa-3.0 de, Bildschön/Peter Lorenz, Montage: biotechnologie.de
Mit dem neuen Bundeskabinett ist nun das Personal benannt, das künftig den politischen Kurs für Themen Biotechnologie, Gesundheitswirtschaft und Bioökonomie mitbestimmen wird.
An der Spitze des Bundesministeriums für Bildung und Forschung (BMBF) gibt es keine personellen Änderungen. Die promovierte Mathematikerin Johanna Wanka (CDU) wird auch in der großen Koalition das Ressort leiten. Änderungen gibt es hingegen auf Ebene der Staatssekretäre: Der bisherige Parlamentarische Staatssekretär Helge Braun (CDU) wechselt als Staatsminister ins Kanzleramt. Nachrücken soll Stefan Müller, der bisher Parlamentarischer Geschäftsführer der CSU-Landesgruppe im Bundestag ist. Thomas Rachel (CDU) bleibt Parlamentarischer Staatssekretär im BMBF. Das Bundesministerium für Ernährung und Landwirtschaft wird zukünftig vom bisherigen Innenminister Hans-Peter Friedrich (CSU) geführt. Als Parlamentarische Staatssekretäre werden Peter Bleser (CDU) und Maria Flachsbarth (CDU) künftig ebenfalls die Landwirtschaftspolitik mitbestimmen. Der Verantwortungsbereich für den Verbraucherschutz wird in das von der SPD geführte Justizministerium verlagert. Personelle Veränderungen gibt es auch im Entwicklungsministerium.
| Mehr auf biotechnologie.de |
Das Ressort fällt an die CSU und wird in den nächsten vier Jahren von Gerd Müller geleitet, der bisher Parlamentarischer Staatssekretär im Agrarministerium war. Vizekanzler und SPD-Parteichef Siegmar Gabriel wird das neu zugeschnittene Bundesministerium für Wirtschaft und Energie übernehmen. Neuer Bundesgesundheitsminister wird der bisherige CDU-Generalsekretär Hermann Gröhe. Die größten Änderungen gibt es beim Umweltministerium. Dem Haus fallen zusätzliche Kompetenzen im Bereich Bau zu, die bisher beim Verkehrsministerium angesiedelt waren. Im Gegenzug gibt es die Verantwortung für den Bereich Energie an das nun von SPD-Chef Gabriel geleitete Wirtschaftsministerium ab. Die Sozialdemokratin Barbara Hendricks wird das Umweltministerium übernehmen.
© biotechnologie.de/bb
Strüngmann-Brüder investieren in Biosimilars
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
- Strüngmann-Investment in Formycon: Rund 400 Millionen Euro Meilensteinzahlungen für das Erreichen aller Ziele sind möglich, heißt es in Branchenkreisen. Quelle: Esther Stosch / pixelio.de
Für einen dreistelligen Millionenbetrag hat sich die Santo Holding GmbH, hinter der die Brüder Strüngmann stehen, die Rechte an einem von der Formycon AG entwickelten Biosimilar gesichert.
Santo übernimmt die Verantwortung und die Kosten für die gesamte Weiterentwicklung, Herstellung sowie die Vermarktung des biotechnologisch hergestellten Nachahmerpräparats. Die Produktentwicklung wird jedoch bis zur Zulassung weiterhin in den Laboren von Formycon durchgeführt, teilte das Unternehmen am 12. Dezember mit. Vorab erhält der Biosimilars-Spezialist eine einstellige Millionensumme. Der Gesamtwert des Vertrages könnte beim Erreichen bestimmter Meilensteine rund 400 Millionen Euro erreichen, heißt es in Branchenkreisen. Formycon selbst bestätigt nur den „Anspruch auf weitere Zahlungen, die im dreistelligen Millionen-Euro-Bereich liegen.“
| Mehr auf biotechnologie.de |
Auch welches Biosimilar genau entwickelt wird, wollten die Projektpartner noch nicht bekannt geben. Formycon hat sich auf die sogenannte dritte Generation von Biosimilars spezialisiert. Der Patentschutz für die davon betroffenen Originalpräparate läuft frühestens 2020 ab. In Frage kämen also beispielsweise das von Novartis vertriebene Augenmittel Lucentis oder der von GlaxoSmithKline entwickelte Antikörper Benlysta gegen die Autoimmunkrankheit Lupus erythematodes. Die Münchener Formycon AG hatte erst im vergangenen Jahr eine grundlegende Restrukturierung des eigenen Geschäfts eingeleitet. Die Firma in ihrer jetzigen Form entstand durch die Übernahme der Dienstleistungs- und Produktionssparte von Scil Technology durch die Nanohale AG im Januar 2012. Seinen bisherigen Arbeitsschwerpunkt, die Formulierung von inhalativen Wirkstoffen gab Nanohale wenige Monate später auf, ebenso den eigenen Namen: Unter der Bezeichnung Formycon konzentriert sich die Firma seitdem auf die Entwicklung von Biosimilars. Offenbar mit Erfolg: Die Brüder Thomas und Andreas Strüngmann gehören zu den aktivsten Biotech-Investoren in Deutschland. Seit dem Verkauf des Generika-Spezialisten Hexal an Teva haben sie rund 800 Millionen Euro in die Branche investiert. In der Vergangenheit bewiesen die Zwillinge bereits ein gutes Gespür für lohnende Investitionen: Der Krebs-Spezialist Ganymed Pharmaceuticals AG hat gerade erst eine weitere Finanzierungsrunde abgeschlossen (mehr…), um die Entwicklung des Krebsantikörpers IMAB362 voranzutreiben. Auch die Aicuris GmbH in Wuppertal, die sich auf die Entwicklung neuer Antiinfektiva konzentriert (mehr…), gehört zum Portfolio.
© biotechnologie.de/bk
Regeneration beim Axolotl molekular entschlüsselt
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
- Axolotl werden biologisch gesehen nie richtig erwachsen. In ausgewachsener Form sind sie geschlechtsreife Larvenstadien, die die Fähigkeit besitzen, Körperteile vollständig zu regenerieren. Quelle: LoKiLeCh/Wikimedia Commons/CC-BY-SA-3.0
Dresdner Entwicklungsbiologen haben wichtige molekulare Details aufgeklärt, durch die mexikanische Salamander verlorene Gliedmaßen nachwachsen lassen.
Axolotl sind unter den Wirbeltieren echte Regenerationswunder: verlorene Gliedmaßen wachsen vollständig und funktionstüchtig wieder nach. Unbekannt war bisher, wie genau der Heilungsprozess auf Zellebene abläuft. Gelöst haben dieses Rätsel nun Entwicklungsbiologen um Elly Tanaka vom DFG-Forschungszentrum für Regenerative Therapien Dresden – Exzellenzcluster an der TU Dresden (CRTD). Im Fachjournal Science (2013, Bd. 324, S. 1375-1379) beschreiben sie, dass fehlende Gliedmaßen durch fortlaufende Spezifizierung beim Axolotl nachgebildet werden.
| Mehr auf biotechnologie.de |
In einem fein abgestimmten Prozess werden zu jedem Zeitpunkt genau die richtigen Zellen gebildet. Nach einer Amputation vermehren sich die verbliebenen Zellen in den ersten sechs Tagen besonders stark. „Zu diesem Zeitpunkt wird ein Gen angeschaltet, das den Zellen mitteilt, dass sie sich auf der verkürzten Seite des Glieds befinden“, berichtet Akira Tazaki vom CRTD. „Wenn wir im Oberarm das Glied durchtrennen, schalten die sich in den ersten sechs Tagen stark vermehrenden Zellen ein Gen an, um den Unterarm nachwachsen zu lassen.“ Nach sechs weiteren Tagen beginnen die sich stark vermehrenden Blastemzellen, die Identität des benachbarten Gliedsegments anzunehmen. Wird also der Oberarm durchtrennt, entwickeln sich zunächst die Zellen für die Bildung des Oberarms, danach diejenigen für den Unterarm. Erst ganz zum Schluss folgen Zellen für die Fingerspitzen. Über die herausragenden Regenerationsfähigkeiten der Schwanzlurche verfügt der menschliche Körper von Natur aus nicht. Trotzdem könnte auch die Medizin von den neuen Erkenntnissen profitieren, hofft Tanaka: „Dieses Wissen erlaubt uns erst, grundsätzlich darüber nachzudenken, wie wir Gewebe von Gliedmaßen entwickeln können.“
© biotechnologie.de/bk
Mikroben faszinieren mit Wasserstoff-Speichertrick
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
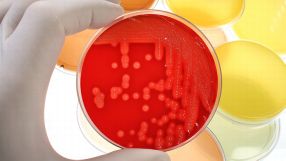
- Die Arbeitsgruppe um Volker Müller untersucht verschiedene Essigsäure produzierende Bakterien auf ihr Potenzial zur Gewinnung von Treibstoffen. Quelle: Julian Rovagnati/fotolia.de
Ein Frankfurter Forscherduo hat in Mikroben ein Enzym aufgespürt, mit dem sich Wasserstoff äußerst effizient in Form von Ameisensäure speichern lässt.
Die Biowissenschaftler Kai Schuchmann und Volker Müller von der Goethe-Universität Frankfurt berichten im Fachjournal Science (2013, Bd. 342, S. 1382) über ihren Fund. Im Bakterium Acetobacterium woodii haben sie ein Enzym entdeckt, das es befähigt, Wasserstoff und Kohlendioxid zu Ameisensäure umzusetzen. So können die Forscher entweder ganze Bakterienzellen oder die isolierte Wasserstoff-abhängige CO2-Reduktase zur Gewinnung von Treibstoffen einsetzen. Die flüssige Variante aus Ameisensäure kann leichter als der gasförmige Wasserstoff gelagert und transportiert werden. „Ein Auto mit Brennstoffzelle benötigt circa 45.000 Liter Wasserstoff für 400 Kilometer. Diese Menge ließe sich in circa 75 Litern flüssiger Ameisensäure speichern“, erläutert Kai Schuchmann.
| Mehr auf biotechnologie.de |
Entdeckt hat der Biowissenschaftler das Enzym im Rahmen seiner Doktorarbeit, in der er sich mit dem Stoffwechsel des Bakteriums beschäftigt. Die biologische Methode zur Gewinnung des Treibstoffs bringt viele Vorteile mit sich. Bislang waren hohe Temperaturen und Drücke sowie chemische Additive in Katalysatoren notwendig, um Wasserstoff und CO2 in Treibstoffe zu verwandeln. „Attraktiv ist das Enzym nicht nur deshalb, weil es sowohl die Speicherung als auch die Freisetzung von Wasserstoff mit hoher Effizienz ermöglicht“, erklärt Volker Müller, an der Uni Frankfurt Leiter der Abteilung für Molekulare Mikrobiologie und Bioenergetik. Sogar die Verwertung von Kohlenmonoxid sei über einen alternativen Weg möglich. Dies sei von Vorteil, da Brennstoffzellen durch Verunreinigungen mit Kohlenmonoxid geschädigt werden können. Bei der Entwicklung des Katalysators mussten die Mikrobiologen eine besondere Herausforderung meistern: A. woodii stellt Ameisensäure nur als Zwischenprodukt her, das in darauf folgenden Stoffwechselschritten weiterverarbeitet wird. In einer früheren Studie fand Volker Müller heraus, dass man dem Bakterium hierfür Natrium-Ionen vorenthalten muss, die es für die Folgereaktionen braucht. Ihre Technologie haben sich die Frankfurter nun patentieren lassen.
© biotechnologie.de/bs