Epigenetischer Geschlechterkampf in der befruchteten Eizelle
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
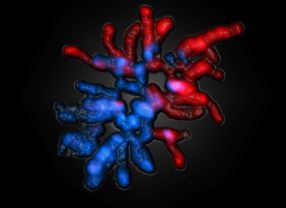
- Mütterliche (blau) und väterliche (rot) Chromosomen am Ende der ersten Zellteilung. Die epigenetischen Markierungen der väterlichen Chromosomen wurden bereits vollständig umprogrammiert. Das mütterliche Erbmaterial ist vor diesem Prozess geschützt. Quelle: Walter / UdS
29.03.2011 -
Welche Gene in einer Zelle abgelesen werden können, ist entscheidend für ihre Eigenschaften. Mit kleinen chemischen Markierungen kann eine Zelle bestimmte Bereiche des Erbguts stilllegen. Forscher um den Saarbrücker Epigenetiker Jörn Walter haben nun aufgedeckt, wie die epigenetischen Markierungen in einer Eizelle kurz nach der Befruchtung völlig neu programmiert werden. Dabei werden offenbar nur die väterlichen Chromosomen wieder auf Null gesetzt, das Erbgut der Mutter ist geschützt. Im Fachblatt Natur Communications beschreiben die Forscher, wie der Resetknopf für Gene funktioniert (Online-Vorabveröffentlichung, 15. März 2011).
Das Schicksal einer Zelle entscheidet sich daran, welche Teile des Erbgutes tatsächlich verwirklicht werden und welche stumm bleiben. Egal ob Nervenzelle im Hirn oder Muskelzelle im Herzen, jede Zelle im menschlichen Körper hat die exakt gleiche genetische Grundausstattung an Bord. Allein dadurch, dass in jedem der mehr als 200 Zelltypen im menschlichen Körper andere Teile des Erbmaterials aktiv sind, entstehen Zellen, die für die unterschiedlichsten Aufgaben spezialisiert sind. Um zu regulieren, welcher Teil der Erbinformation gerade genutzt werden soll, kann die Zelle die DNA mit kleinen chemischen Molekülen markieren und so die Lesehäufigkeit herauf- oder herabsetzen. Die häufigste dieser epigenetischen Markierungen ist die Methylierung, bei ihr wird eine Methylgruppe an die DNA geheftet. Mit der Erforschung dieser programmierbaren An- und Abschalt-Automatik beschäftigt sich die Epigenetik. Dezeit laufen weltweit Forschungsprojekte, um die Rolle der Epigenetik für die Vererbung besser zu verstehen. Im „International Human Epigenome Consortium (IHEC)“ koordinieren Forscher ihre Anstrengungen. Das ehrgeizige Ziel: In den kommenden Jahren sollen 1000 genetische „Fingerabdrücke“ von jedem menschlichen Zelltyp angefertigt werden (mehr…). Auch Walter ist Mitglied in diesem internationalen Verbund. In seinem aktuellen Projekt zeigt er, welche wichtige Rolle die Epigentik schon beim Entstehen neuen Lebens spielt.
| Mehr auf biotechnologie.de |
News: Epigenetische Medikamente - Präzisionsgewehr statt Schrotflinte News: Freiburger Max-Planck-Institut trägt nun Epigenetik im Namen Menschen: Heinrich Leonhardt - Entschlüsselung des epigenetischen Codes |
„Kontrollierte epigenetische Decodierung von zentraler Bedeutung“
Zum Beginn eines neuen Lebens, beim Verschmelzen der elterlichen DNA in der befruchteten Eizelle, werden die epigenetischen Markierungen vollständig reprogrammiert. Wie genau das passiert, hat jetzt erstmals ein internationales Forscherteam um Jörn Walter von der Universität des Saarlandes beschrieben. Sie untersuchten dafür die noch nicht miteinander verschmolzene Eltern-DNA in den befruchteten Eizellen von Mäusen, Kühen und Kaninchen. „Damit sich ein Embryo normal entwickeln kann, ist eine kontrollierte epigenetische Dekodierung des mütterlichen und väterlichen Erbmaterials kurz nach der Entstehung neuen Lebens von zentraler Bedeutung“, erklärt Walter.
Diese „epigenetische Reprogrammierung“ entdeckte das Team um den Saarbrücker Biologen schon vor geraumer Zeit. Das Löschen der an der DNA angebrachten chemischen Modifizierungen ist unbedingt notwendig. Nur so erhalten die Zellen im sich entwickelnden Embryo wieder die Fähigkeit, sich aus einer Stammzelle in alle Zelltypen zu entwickeln, die in einem Körper vorhanden sind. Damals entdeckten die Forscher einen erstaunlichen Unterschied: Während väterliche, aus dem Spermium stammende Chromosomen rasch reprogrammiert wurden, schien sich das mütterliche, aus der Eizelle stammende Erbgut vor diesem Schritt zu schützen.
Protein Stella sorgt für „den kleinen Unterschied“
Nun ist es Walter gemeinsam mit Kollegen von den Universitäten Cambridge (Großbritannien) und Osaka (Japan) gelungen, den Mechanismus aufzuklären, der hinter diesem Resetknopf für Gene steht. Ein erster Schritt ist offenbar das Modifizieren eines epigenetischen Faktors mit dem Namen 5-Methylcytosin (5mC) in den väterlichen Chromosomen. Ihm wird eine weitere kleine Molekülgruppe angeheftet, so dass 5-Hydroxy-Methylcytosin (5hmC) entsteht. Verantwortlich für diesen Schritt ist wohl das Enzym Tet3. Sobald die Forscher um Walter die Bildung dieses Enzyms gehemmt hatten, stoppte auch die Reprogrammierung der väterlichen Chromosomen.
Die nächste Frage, die sich das Team stellte, war naheliegend: Warum sind die mütterlichen, aus der Eizelle stammenden Chromosomen vor diesem Reset geschützt? Die Antwort: Das Protein Stella sorgt für „den kleinen Unterschied“. Fehlte den Eizellen dieses Protein, so wurde auch ihr Erbgut von Tet3 umgeschrieben. Die Schlussfolgerung der internationalen Forschergruppe: Die mütterliche Eizelle bestimmt mit sehr ausgeklügelten epigenetischen Werkzeugen über die Interpretation des väterlichen Genoms.
Epigenetische Programmfehler beeinflussen Volkskrankheiten
Bereits vor zehn Jahren hatten die Wissenschaftler diesen Kampf der Geschlechter beschrieben – aber erst jetzt sind sie den Mechanismen auf die Spur gekommen. „Die schnelle Reprogrammierung der epigenetischen Information des väterlichen Genoms erfüllt vermutlich zwei Aufgaben“, erläutert Walter. „Zum einen werden die epigenetischen Fehler des Vaters gelöscht. Zum anderen wird das Genom für die Vielzahl der neuen Aufgaben vorbereitet, die für eine totipotente, also vollständige Entwicklung wichtig sind.“
Besondere Bedeutung haben ihre Erkenntnisse für Stammzellforscher, die versuchen, adulte oder fetale Zellen in entwicklungsfähige Stammzellen zu verwandeln. Solche Zellen werden nicht von Embryonen gewonnen, sondern können aus dem Gewebe von Erwachsenen oder Neugeborenen (zum Beispiel Fettgewebe oder Nabelschnurblut) isoliert werden. Sie sind aber zunächst weniger vielseitig als embryonale Stammzellen, können aber im Labor in voll entwicklungsfähige Stammzellen umgewandelt werden.
Aber auch die Behandlung vieler Volkskrankheiten könnte durch die neuen Erkenntnisse beeinflusst werden, glaubt der Saarbrücker Epigenetiker: „Da epigenetische Programmfehler in unmittelbarem Zusammenhang mit der Entstehung komplexer Erkrankungen wie Krebs, Immun- und Stoffwechselerkrankungen oder neuronalen Erkrankungen zu sehen sind, haben die von uns gefundenen Mechanismen eine vermutlich viel weitreichendere Bedeutung als „nur“ für die Steuerung erster Lebensvorgänge.“