Wochenrückblick KW 03
Rückblick auf Kalenderwoche 3
Für den Zeitraum vom 14. bis 21. Januar 2013 hat biotechnologie.de für Sie die wichtigsten Nachrichten aus der Biotech-Branche zusammengestellt.
Gen beeinflusst stressbedingte Alkoholsucht
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
- Bei Mäusen beeinflusst ein Gen für das Enzym Nepilysin den Alkoholkonsum unter Stress.
Leipziger und Berliner Pharmakologen haben bei Mäusen ein Gen entdeckt, das bei der Entstehung von stressbedingter Alkohol-Abhängigkeit eine wichtige Rolle spielt.
Nach Ansicht der Forscher sind ihre Erkenntnisse auf den Menschen übertragbar und könnten zu einer neuen Behandlungsmethode für Betroffene führen. Wie sie in im Fachjournal PLoS One (2013, Online-Veröffentlichung) berichten, steht das Enzym Neprilysin im Zentrum des Suchtmechanismus. Bekannt ist, dass Neprilysin auch bei der Entstehung von Alzheimer und Fettleibigkeit seine Finger im Spiel hat. Für die Alkoholismus-Studie untersuchten die Wissenschaftler um Thomas Walther von der Universität Leipzig Mäuse, denen das Gen für Neprilysin fehlt. Im Experiment konnten die Tiere frei zwischen Flaschen mit Wasser und mit Alkohol wählen. Danach wurde ein fremdes Männchen für maximal 15 Minuten mit in den Käfig gesetzt, was Mäuse unter sehr großen Konkurrenzstress setzt. In dieser Situation fingen sie an, sich verstärkt dem Alkohol zuzuwenden, und zwar in einem Verhältnis, das dem eines Alkoholikers vergleichbar ist.
| Mehr auf biotechnologie.de |
Wochenrückblick: Drogenfeste Fische liefern genetisches Set für Anti-Suchtpotenzial Wochenrückblick: Gene für Internetsucht gefunden Wochenrückblick: Der Kokain-Synthese auf der Spur |
Blieb es bei einer einmaligen Stresssituation, so normalisierte sich der Alkoholkonsum nach einigen Tagen wieder. Wurden sie dagegen ein weiteres Mal gestresst, tranken sie bis zum Abbruch des Experiments exzessiv Alkohol.
„Der Zusammenhang zwischen der Neprilysin-Aktivität und stressbedingtem Alkoholkonsum ist jetzt hergestellt. Wir haben die Befunde sowohl in genetisch veränderten, als auch in pharmakologisch behandelten Tieren erhalten, was die Ergebnisse besonders stark macht“, so Walther. Mittlerweile ist das Team bereits einen Schritt weiter. Die Idee der Forscher: Wenn das Fehlen des Enzyms bei Mäusen deren Suchtanfälligkeit erhöht, dann könnte eine zu geringe Enzymaktivität bei manchen Menschen einen ähnlichen Effekt hervorrufen. In der Tat hat Walthers Team einen ersten hoffnungsvollen Wirkstoff gefunden, der das Enzym Neprilysin aktiver machen kann. Für Walther ist dies ein Fingerzeig in die richtige Richtung: „Auch wenn es bis zur Anwendung beim Patienten noch ein weiter Weg ist, könnte bei Alkoholikern in Zukunft mit Medikamenten auf den Proteinstoffwechsel und damit auf die Sucht eingewirkt werden.“
© biotechnologie.de/ml
Membranproteine falten sich per Reißverschluss-Prinzip
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
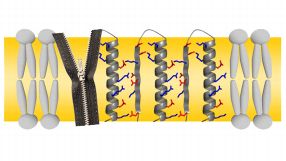
- Das Protein Twin-Arginine Translocase (Tat) formt in Membranen Poren, die nach dem Reißverschluss-Prinzip entstehen. Quelle: KIT
Spezielle Eiweißmoleküle in Biomembranen nutzen einen Reißverschluss aus Ladungen, um sich richtig zu falten und eine Pore zu formen.
Das haben Forscher des Karlsruher Institutes für Technologie (KIT) zusammen mit italienischen Kollegen entdeckt. Sie berichten im Fachmagazin Cell (2013, Bd. 152, S.316). „Ein ‚Ladungsreißverschluss‘ zwischen geladenen Seitenketten ist ein ganz unerwarteter Mechanismus, wie Membranproteine ihre Ladungen neutralisieren und auf diese Weise hydrophobe Zellmembranen durchspannen können“, so Anne Ulrich vom Institut für Biologische Grenzflächen. In der aktuellen Studie untersuchten die KIT-Forscher ein Protein mit dem Namen Twin-Arginine Translocase (Tat). Sie dient in der Zellmembran von Bakterien als Export-Maschine für gefaltete Proteine. Mehrere Exemplare des Bausteins TatA lagern sich zu einer Pore zusammen und können dabei den Durchmesser der Pore flexibel an die zu transportierende Fracht anpassen. Um zu klären, wie eine TatA-Pore entsteht, haben die Forscher den molekularen Aufbau von TatA im Bakterium Bacillus subtilis untersucht. Das Eiweißmolekül besteht aus einer Kette von 70 Aminosäuren. Die Strukturanalyse hat gezeigt, dass sie sich zu einer starren, stäbchenförmigen Helix auffaltet, auf die ein sehr geschmeidiger, langgestreckter Bereich folgt. Viele der Aminosäuren in der Helix und im angrenzenden Bereich tragen negative oder positive Ladungen, die einer Ionenladung entsprechen. „Erstaunlicherweise ist die Reihenfolge der Ladungen auf der Helix komplementär zu denen im angrenzenden Bereich des Proteins“, sagt Ulrich.
| Mehr auf biotechnologie.de |
News: Calcium-Express: Turbo-Schalter bei Zellpumpe entdeckt Wochenrückblick: Funktion eines Bakterien-Kanals aufgeklärt |
Klappt man das Protein also an der Verbindungsstelle zusammen wie ein Scharnier, treffen immer positive und negative Ladungen aufeinander und ziehen sich an. Das Protein verbindet also seine beiden Bereiche so, wie die Zähne eines Reißverschlusses ineinandergreifen. „Der Clou ist jedoch, dass dieses Bindungsprinzip auch gegenüber den Nachbarproteinen funktioniert“, erklärt Ulrich. Statt sich also ganz alleine zuzuklappen, geht jedes TatA Protein auch Reißverschlussbindungen mit seinen beiden Nachbarn ein. Wie Computersimulationen zeigen, entstehen dadurch stabile und zugleich flexible Verbindungen zwischen den benachbarten Molekülen. Dieses neuartige Reißverschlussprinzip scheint nicht nur beim Proteintransport eine Rolle zu spielen, sondern auch beim Angriff bestimmter antimikrobieller Peptide auf Bakterien oder bei deren Stressantwort durch Biofilmbildung.
© biotechnologie.de/pg
Qiagen baut Test-Palette aus
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
- Qiagen hat die Zulassung eines therapiebegleitenden Tests bei der FDA beantragt. Quelle: Qiagen
Der Hildener Diagnostik-Spezialist Qiagen baut seine Palette an therapiebegleitenden Testverfahren weiter aus.
Das Unternehmen hat die Arbeiten an einem therapiebegleitenden Diagnostikum für ein neues Lungenkrebs-Medikament abgeschlossen und beantragt bei der der US-Behörde FDA die Zulassung. Der Hildener Konzern kooperiert hierbei mit dem Pharma-Unternehmen Boehringer Ingelheim, um den molekulargenetischen Nachweis als Begleittest (Companion Diagnostic) für das Präparat Afatinib zu entwickeln. Der Tyrosinkinase-Inhibitor von Boehringer soll zur Behandlung von Patienten genutzt werden, die an einem lokal fortgeschrittenen oder metastasierenden nicht-kleinzelligen Lungenkrebs leiden, welcher eine Mutation im Gen für den epidermalen Wachstumsfaktors (EGFR) aufweist. In den Indikationen Arthritis, Lungenkrebs sowie Darmkrebs hat sich das Hildener Unternehmen in den vergangenen Wochen zudem den Zugriff auf neue Biomarker gesichert. Biomarker sind Moleküle, die bei Patienten etwas über Krankheitsverlauf und Therapieerfolg verraten. Ihre Vermessung sollen künftig genutzt werden, um die für den jeweiligen Patienten optimale Therapieentscheidung zu treffen. Zu diesem Zweck sollen die meisten der nun einlizenzierten Tests auf die hauseigene Automatisierungsplattform angepasst werden.
| Mehr auf biotechnologie.de |
Wochenrückblick: FDA genehmigt Qiagen-Grippetest Wochenrückblick: Humangenetiker verteidigen Pränataltest auf Trisomie 21 |
Qiagen scheint es nun vor allem ein von der Drug Response Dx GmbH (DRDx) einlizenziertes Testkit zur richtigen Behandlung von Rheumatoider Arthritis angetan zu haben. Unternehmenschef Peer Schatz betonte, dieser Satz an Biomarkern würde die Therapie der weit verbreiteten Krankheit entscheidend verändern. Gemeinsam mit dem Hightech-Gründerfonds stieg Qiagen kürzlich bei dem in Hennigsdorf ansässigen Start-up ein. Das dort entwickelte DRDx-Testkit soll eine individuelle Wirksamkeitsvorhersage für sogenannte TNF-Alpha-Inhibitoren für Arthritis-Patienten bereits vor Medikamentengabe ermöglichen. Für das antikörperbasierte Nachweisverfahren liege bereits ein Machbarkeitsnachweis vor. Als nächstes soll das Diagnostikum klinisch geprüft werden. Von der US-amerikanischen Insight Genetics sicherte sich Qiagen zudem die weltweiten exklusiven Rechte für drei Biomarker zur Untersuchung von nicht-kleinzelligem Lungenkarzinom, der häufigsten Form von Lungenkrebs. Die aus der übernommenen Ipsogen hervorgegangene Tochtergesellschaft Qiagen Marseille wurde hingegen bei InsermTransfert, der Technologietransfer-Sparte der französischen Forschungsorganisation Inserm fündig. Ein Biomarker für Mutationen des HSP110-Gens soll dabei helfen, die sogenannte Mikrosatelliteninstabilität zu erkennen, die bei etwa 15 Prozent aller Darmkrebs-Patienten auftritt.
© biotechnologie.de/bk
Aussaat von Gentech-Weizen in Üplingen verschoben
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
- Die geplante Aussaat von gv-Weizen in Üplingen verschiebt sich wegen schlechter Witterung. Quelle: Schaugarten Üplingen
Aufgrund der schlechten Witterung ist die Aussaat von gentechnisch verändertem Winterweizen in Üplingen auf den Herbst verschoben worden.
Die anhaltend schlechten Bodenbedingungen in den vergangenen Wochen hätten eine Aussaat der gv-Saat auf dem Versuchsgelände verhindert, teilte das Leibniz-Insitut für Pflanzengenetik und Kulturpflanzenforschung (IPK) in Gatersleben am 16. Januar mit. Das IPK will in dem Projekt Studien zum Ertrag und den Korneigenschaften von genetisch verändertem Winterweizen unter Freilandbedingungen analysieren. Der Weizen, in den Gene und Genelemente aus Gerste eingebracht wurden, weist nach Angaben der Forscher einen deutlich höheren Korn- und Proteinertrag auf. Die Forscher wollten 236 verschiedene Kreuzungslinien anbauen, um ertragsrelevante Parameter zu erfassen und Kornproben im Labor zu untersuchen. Anfang Dezember 2012 hatte das Bundesamt für Verbraucherschutz und Lebensmittelsicherheit (BVL) die Genehmigung zur Freisetzung der gv-Weizenlinien in den zwei Vegetationszeiträumen für 2013 und 2014 in Üplingen erteilt. Im Ergebnis ihrer Überprüfung kamen die Experten zu dem Schluss, dass der Versuch mit den Winterweizenlinien, die keine Marker- und Resistenzgene enthalten, weder Menschen noch Tiere gefährdet und keine Gefahr für die Umwelt darstellt.
| Mehr auf biotechnologie.de |
Wochenrückblick: Schweiz: GVO-Moratorium auf dem Prüfstand |
Die Gaterslebener Forscher wollten auf einer Gesamtfläche von zehntausend Quadratmetern auf dem Gelände der BioTechFarm GmbH und Co KG in Üplingen 43.020 transgene Pflanzen und nicht veränderte Kontrollpflanzen anbauen. Im Gewächshaus ließ sich bei den Winterweizenlinien eine Erhöhung des Korn- und Proteinertrages um etwa 20 Prozent beobachten. „Das ist für uns Motivation genug, die besonderen Mühen einer Freisetzung auf uns zu nehmen. Wir werden in den kommenden Monaten alle Vorbereitungen treffen und die Aussaat im Herbst 2013 vornehmen“, erläutert die Projektleiterin Winfriede Weschke. Ein ähnlicher Versuch der Gaterslebener Forscher war im April 2008 von sechs Antigentechnikaktivisten zerstört worden. Der Verlust von mehr als 50 Prozent der Pflanzen verhinderte die Auswertung mit entsprechenden Konsequenzen für die beteiligten Wissenschaftlerinnen und Wissenschaftler. Mittlerweile sind die Aktivisten in einem Strafverfahren verurteilt worden.
© biotechnologie.de/pg