Alzheimer berechenbarer machen
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
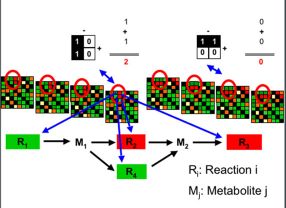
- Die Grafik veranschaulicht die Methode von PathWave - ein Auswertungssystem, welches den Stoffwechsel der Nervenzellen abbildet. Quelle: Rainer König
08.03.2011 -
Alzheimer ist eine der häufigsten neurodegenerativen Erkrankungen der Welt. Die nach dem Wissenschaftler Alois Alzheimer benannte Demenzerkrankung äußert sich durch einen fortschreitenden Verlust der kognitiven und später auch motorischen Fähigkeiten. Obwohl es einen Katalog an Frühwarnzeichen gibt, ist bis heute nicht eindeutig geklärt, wie die Krankheit entsteht. Ein Konsortium aus deutschen und amerikanischen Wissenschaftlern hat jetzt ein neues Modell erstellt, welches die Stoffwechselprozesse im Gehirn abbildet. Damit hofft die vom Nationalen Genomforschungsnetz (NGFN), einer Förderinitiative des Bundesforschungsministeriums, geförderte Kooperation, die Krankheit besser zu verstehen und neue Therapiemöglichkeiten zu finden.
Mehr als 700.000, meist ältere Menschen, sind allein in Deutschland von Alzheimer betroffen. Während es inzwischen einen umfangreichen Katalog an Frühwarnzeichen gibt, sind die genauen Ursachen bisher ungeklärt. Verschiedene Experimente haben jedoch gezeigt, dass sich die Stoffwechselraten in verschiedenen Hirnregionen bereits einige Jahre vor dem Einsetzen erster Krankheitssymptome verändern.
| Mehr zum Thema auf biotechnologie.de |
News: Neurodegenerative Erkrankungen: Ungewöhnliche Allianzen gefragt Menschen: Susann Schweiger: Pendelt zwischen den Welten Menschen: Paul Saftig: Die Alzheimer-Scheren stumpfer machen |
Wissenschaftler der University of California in San Diego in den USA und der Universität Heidelberg haben zusammen ein bioinformatisches Modell erstellt, mit dem sie Stoffwechselwege zwischen verschiedenen Zelltypen vorhersagen können. Auf diesem Weg haben sie Stoffwechselreaktionen verschiedener Nervenzell-Typen und die Aktivität von insgesamt 400 Genen erfasst.
Gleichungen für die Enzyme
Das Modell ist dabei keine plastische Darstellung, sondern ein mathematisches Gleichungssystem, mit dem die Stoffwechselprozesse eines Enzyms dargestellt werden. Je nach Enzym verändern sich die Rahmenbedingungen – bei 400 Genen, die Enzyme kodieren, entsteht ein umfangreiches Gleichungssystem mit über 900 Gleichungen, welches die Prozesse in einer Zelle abbildet. „Wir haben eine Auswertungsmethode entwickelt, um experimentell ermittelte Genexpressionsdaten mit diesem Modell zu vergleichen,“ erläutert Rainer König, Leiter der institutsübergreifenden Arbeitsgruppe aus Wissenschaftlern von BioQuant, Universität Heidelberg
und dem Deutschen Krebsforschungszentrum (DKFZ). Will heißen: Die Forscher untersuchen mit diesen Daten das Vorkommen bestimmter Enzyme im Gehirn verstorbener Alzheimer-Patienten, und vergleichen die Befunde mit den Lösungen aus dem Gleichungssystem.
Mit Hilfe des jetzt neu entwickelten Auswertungssystems PATHWAVE haben König und sein Team zusammen mit den Amerikanern herausgefunden, dass bei Alzheimer-Patienten der Energiestoffwechsel in manchen Hirnregionen stark vermindert ist. Der Grund: Ein Schlüsselenzym, die Alpha-Ketoglutarat- Dehydrogenase, arbeitet nur noch eingeschränkt.
Der Prozess wird umgeleitet
Überraschend waren dabei die Untersuchungsergebnisse von Nervenzellen, die in der pathologischen Untersuchung keinerlei Auffälligkeiten gezeigt hatten. „Diese Stoffwechselprozesse, die den Zellhaushalt stören, finden auch in äußerlich nicht betroffenem Gewebe statt“, resümiert König. Des Rätsels Lösung liegt in einem anderen Enzym. Es sorgt dafür, dass ein anderer Nervenzelltyp diesen Aktivitätsverlust durch eine Umleitung der Stoffwechselflüsse ausgleicht, so dass die Nervenzellen wie gewohnt weiter funktionieren. Den Wissenschaftlern zufolge regelt diesen Umleitungsprozess
In der 72. Folge von biotechnologie.tv geht es unter anderem um neue Strategien gegen Alzheimer.Quelle: biotechnologie.tv
die Glutamat-Dehydrogenase (GAD). Diese mathematische Erklärung wird unterstützt durch vorhergehende Studien und Untersuchungen an verstorbenen Alzheimer-Patienten. In ihrem Gehirn fand sich in geschädigten Regionen besonders wenig GAD – der Umleitungsmechanismus hatte nicht funktioniert.
Vielfältig anwendbares Modell
„Besonders spannend ist, dass unser Modell bekannte Phänomene bestätigt und wir außerdem neue Schlüsse ziehen können, die relevant für die Erkrankung sind“, sagt Rainer König. Die Methode ist vielfältig einsetzbar. Da König am Deutschen Krebsforschungszentrum angesiedelt ist, will er die Auswertungsmethode vor allem einsetzen, um Tumore zu erforschen. Doch in der Bioinformatik müssten zuerst die Zahlen stimmen, die Erkrankung sei dabei erst in zweiter Linie relevant. Je besser das Modell, desto präzisere Vorhersagen könnten über den Krankheitsverlauf getroffen werden. Die Schlüsse aus den Analysen der Gleichungen und der experimentellen Daten bilden damit den ersten Schritt zu einer möglichen Behandlung der bisher unheilbaren Krankheit.