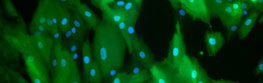
Die Alge baut das Wunschprotein
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
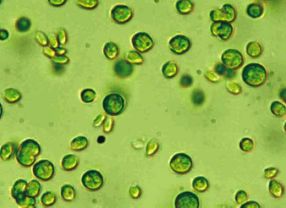
- Winzige Proteinfabriken: Lichtmikroskopische Aufnahme der Mikroalge "Chlamydomonas reinhardtii". Quelle: Olaf Kruse/ Universität Bielefeld
26.07.2011 -
Um biologische Medikamente herzustellen, werden in der Regel Bakterien oder auch Säugetierzellen benutzt. Da Bakterien jedoch keine hochkomplexen Proteine herstellen können und weil Säugtierzellen teuer sind, geraten immer mehr auch Pflanzenzellen als Biofabriken in den Fokus. In Münster, dem schwedischen Umea, in Madrid und dem französischen Rouen beschäftigt sich eine Forschungskooperation mit den Möglichkeiten der Proteinbiosynthese in Grünalgen. ALGALGLYCO nennt sich die Kooperation, die vom Bundesministerium für Bildung und Forschung innerhalb der Förderinitiative KMU-innovativ über drei Jahre mit insgesamt 545.000 Euro gefördert wird.
Im ALGALGLYCO-Verbund wollen die Forscher Glykoproteine herstellen, eine Klasse von Eiweißen, die zusätzlich mit einer Struktur von Mehrfachzuckern (Oligosacchariden) umgeben sind. Glykoproteine kommen bei höher entwickelten Säugetieren und natürlich dem Menschen vor. Die Zuckerschicht stabilisiert das Protein und verändert seine physiochemischen Eigenschaften erheblich, sodass zum Beispiel ein Impfstoff an die Zelle andocken kann. Da es die Glycosilierung von Proteinen im Endoplasmatischen Reticulum (ER) stattfindet, einer Organelle, die nur prokaryotische Organismen besitzen, scheiden Bakterien und Hefen als Biofabriken aus.
| AG Biochemie der Pflanzen |
Michael Hippler leitet am Institut für Biologie und Biotechnologie der Pflanzen der Universität Münster eine Arbeitsgruppe. zur AG: hier klicken |
ALGALGLYCO haben deshalb Clamydomonas rheinhardtii im Visier, eine einzellige Grünalge. Grünalgen sind in ihrer Eignung als winzige Produktionsstätten sozusagen die Hefen unter den pflanzlichen Biofabriken. Bereits 2007 wurde ihr Genom entschlüsselt, durch das einfügen bestimmter Gensequenzen lässt sich Clamydomonas zur Produktion ganz unterschiedlicher Proteine anregen. Anders als die ebenfalls als grüne Biofabrik genutzte Ackerschmalwandpflanze Arabidopsis thaliana werden Algen jedoch in Petrischalen gezüchtet. Das hat Vorteile. „Das ist ein abgeschlossenes System“, sagt Michal Hippler, Professor für pflanzliche Biochemie an der Universität Münster, der das Projekt von deutscher Seite koordiniert. „Man bekommt da keine Probleme mit der Freisetzung transgener Pflanzen.“
Wunschproteine in Chloroplasten zwischenlagern
Hippler und seine Kollegen untersuchen, inwieweit Clamydomonas für die Produktion der begehrten Glykoproteine geeignet ist. „Uns geht es vor allem darum herauszufinden, inwieweit glykosilierte Proteine schon natürlich in den Algen zu finden sind und wie diese Proteine, die im Kern codiert sind, in die Chloroplasten kommen“, sagt Hippler. Den gleichen Pfad wollen die Wissenschaftler ausnutzen, um in den Grünalgen zunächst humane „Wunsch-Proteine“ zu synthetisieren und sie anschließend in den Chloroplasten zu sammeln. Diese dienen als Speicher, dort gelagerte Proteine werden nicht wie anderswo in der Zelle schnell wieder abgebaut. Dass der Trick grundsätzlich funktioniert, wissen die Forscher bereits aus Versuchen mit Arabidopsis.
| KMU-innovativ |
Im Jahr 2007 erweiterte das BMBF die erfolgreichen Förderinitiativen BioChance und BioChancePlus. Unter dem Titel "KMU-innovativ" werden nun kleine und mittlere Unternehmen unterstützt, die besonders aufwendige Forschungen betreiben. Insgesamt 300 Millionen Euro stehen bis zum Jahr 2015 für zunächst fünf Technologiefelder zur Verfügung. Mehr Informationen zur Förderinitiative auf biotechnologie.de: hier klicken |
In einem ersten Schritt haben die Molekularbiologen erforscht, welche Grünalgen überhaupt glykosilierte Proteine herstellen können. „Wir haben schon verschiedene gefunden, die Liste vergrößert sich ständig“, sagt Hippler. Im Augenblick sehen sich die ALGALGLYCO-Forscher an, wie die glykosilierten Proteine aus dem Endoplasmatischen Retikulum in die Chloroplasten gelangen. „Wir versuchen zu verstehen, welche Enzyme dazu benötigt werden“, sagt Hippler. Die nächste Frage ist: „Wie sieht die Struktur der Glykoproteine in Clamydomonas aus?“ Ist das bekannt, kann durch genetische Modifikation der Alge auch das Protein verändert werden. „Am Ende des Tages möchte man natürlich sein Wunsch-Glykoprotein bauen“, sagt Hippler.
Arbeitsteilung im internationalen Team
In dem internationalen Verbund bringt jede Arbeitsgruppe spezielle Kenntnisse ein. Der spanische Biochemiker und Molekularbiologe Arsenio Villareja hat die Proteinsynthese in Pflanzen mitentwickelt und war in dem Team der Experte für die Grünalgenart Clamydomonas rheinhardtii. Im Mai 2011 ist er nach einer kurzen Krankheit gestorben. „Wir vermissen ihn sehr“, sagt Hippler. „Seine Arbeit wird jetzt in Madrid von Flor Martinez fortgeführt.“ Auf französischer Seite erforscht die Wissenschaftlerin Muriel Bardor seit 10 Jahren den Mechanismus der N-Glykosilierung in Pflanzen. Hippler und sein 20-köpfiges Team aus Münster sind die Proteom-Experten in der Kooperation und damit vor allem in der Identifikation der Glykoproteine tätig. An der Molekularbiologie der Universität Münster wird seit mehreren Jahren an Herstellungsmethoden für die komplexen Glykoproteine gearbeitet.
Ende 2012 will ALGALGLYCO ein Verfahren entwickelt haben, um Glykoproteine in Algen herzustellen und in Chloroplasten anzusammeln. Dazu sollen die Struktur der Zuckerschicht auf den Grünalgenproteinen und der Glykosilierungsprozess erforscht und beschrieben sein. Interessenten für die Erkenntnisse gibt es bereits. Mehrere Biotechnologieunternehmen haben Hippler zufolge Interesse an den Forschungsergebnissen bekundet.
Autorin: Cornelia Kästner