Blick in die Welt der Membranproteine
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
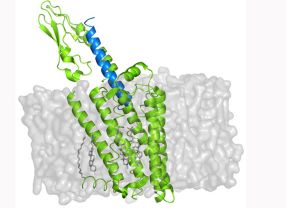
- Die Struktur von derartigen Membranproteinen wollen die HALOmem-Forscher aufklären. Weil sich Membranproteine nur schwer kristallisieren lassen, ist ihre Struktur noch weitgehend unerforscht. Quelle: HALOmem
05.10.2010 -
Wie ein schützender Film legt sich um jede lebende Zelle eine Biomembran. Sie schützt das Zellinnere vor Einflüssen von außen und erhält so das innere Milieu aufrecht. Damit die Zelle mit ihrer Umgebung trotzdem in Kontakt treten kann, verankert sie bestimmte Proteine in ihrer Membran, die als Verbindungsstellen dienen. Die Struktur dieser Membranproteine wollen Forscher im interdisziplinären Forschungszentrum „HALOmem“ in Halle jetzt genauer untersuchen. Zusammen mit dem Land Sachsen-Anhalt stellt das Bundesministerium für Bildung und Forschung im Rahmen des Förderprogramms "Unternehmen Region" bis 2014 insgesamt 9 Millionen Euro zur Förderung des neuen Zentrums zur Verfügung.
Die Bedeutung der Membranproteine ist immens. Sie erst geben der Zelle die Möglichkeit, mit ihrer Umwelt in Kontakt zu treten und Stoffe oder Reize auszutauschen. Ohne sie könnten Nervenzellen nicht miteinander kommunizieren, Hormone hätten keine Wirkung auf die Keimzellen. Auch die moderne Medizin wäre ohne Membranproteine nicht vorstellbar: Zwei von drei Medikamenten wirken, indem sie diese Eiweiße beeinflussen.
| Mehr zum Thema auf biotechnologie.de |
News: Eiweiße in drei Dimensionen sehen Wochenrückblick KW26: Struktur des größten Proteinkomplexes der Atmungskette aufgeklärt. News: Riesiges Atmungsprotein mit einer Million Atomen durchleuchtet |
Wissen über Membranproteine begrenzt
Trotz ihrer offensichtlichen pharmazeutischen und biologischen Bedeutung ist das Wissen über Membranproteine begrenzt. Obwohl es nach Schätzungen mehrere zehntausend verschiedene dieser Membranproteine geben könnte, sind gerade einmal hundert dieser Moleküle in ihrer genauen Zusammensetzung bekannt. Der Grund: Sie lassen sich nur schwierig analysieren. Die meisten Proteine können nämlich nur untersucht werden, wenn sie sich in einer Lösung befinden. Gerade die Membranproteine widersetzen sich jedoch solcherlei Bemühungen der Strukturbiologen: Sie sind kaum wasserlöslich, werden sie doch normalerweise in die fettreichen Zellmembranen eingebaut. Trennt man sie mit Lösungsmitteln aus der Membran heraus, bilden sie häufig keine Proteinkristalle mehr, die wiederum für weitergehende Studien benötigt werden.
Dabei sind genaue Kenntnisse über den Aufbau und die Funktionsweise dieser Proteine Vorraussetzung für die Entwicklung vieler Medikamente. An der Martin-Luther-Universität Halle-Wittenberg haben sich jetzt Wissenschaftler der Institute für Biochemie und Biotechnologie sowie für Physik und Chemie zusammengetan, um neue Membranproteine zu analysieren. „Ist das Zielmolekül eines potentiellen Wirkstoffs auf atomarer Ebene bekannt, kann der oft langwierige Prozess der Entwicklung von Therapeutika ganz entscheidend verkürzt werden“, sagt Milton Stubbs (mehr...), Professor für Physikalische Biotechnologie am Institut für Biochemie und Biotechnologie und zusammen mit Jochen Balbach und Daniel Huster ein Gründer des interdisziplinären Forschungszentrum HALOmem. Untergebracht ist das Zentrum in Räumen des Instituts für Biochemie und Biotechnologie, die eigens für die Bedürfnisse der Forscher umgebaut wurden.
„HALOmem – membrane protein structure & dynamics“ wird bereits seit 2008 vom BMBF unter dem Dach der Förderinitiative „Zentren für Innovationskompetenz“ unterstützt, die zum Programm "Unternehmen Region" ghört und sich auf die Förderung von Forschungstrukturen in den Neuen Bundesländern verschrieben hat. Zusammen mit dem Land Sachsen-Anhalt werden nun bis 2014 neun Millionen Euro zur Verfügung gestellt.
Zentren für Innovationskompetenz |
Im Rahmen des Förderprogramms "Unternehmen region" fördert die Initiative "Zentren für Innovationskompetenz" seit 2004 ausgewählte Forschungsprojekte in den ostdeutschen Ländern, um sie zu international konkurrenzfähigen Zentren auszubauen. In zwei Förderrunden wurden für 14 Projekte bisher rund 220 Millionen Euro bis 2016 bereitgestellt. Mehr Informationen: hier klicken |
Zwei Nachwuchsgruppen erforschen die Membranproteine
Einen Grundstein für die Leistungsfähigkeit des Zentrums sollen eine Auswahl an seltenen Großgeräten legen. Um die Kristallisation von Proteinen beobachten zu können, hat sich der Leiter einer der beiden Nachwuchsgruppen, Mikio Tanabe, zum Beispiel einen ganz besonderen Roboter beschafft. Der „Lipidic Cubic Phase Kristallisationsroboter“ ist der einzige seiner Art in Deutschland. Mit seiner Hilfe wollen die Strukturbiologen Proteinkristalle züchten, um sie später genauer untersuchen zu können. Indem sie beobachten, wie die Kristalle Röntgenlicht streuen, hoffen sie Rückschlüsse auf den Aufbau der Proteine ziehen zu können.
Auf die Frage, wie sich die fertigen Proteine in der Zellmembran verhalten, konzentriert sich eine zweite Nachwuchsgruppe um Kirsten Bacia. Für ihre Untersuchungen nutzt sie ein Fluoreszenz-Korrelationsspektroskopie- und Laser-Raster-Mikroskop (FCS/LSM). „Mit dem Gerät lässt sich die Beweglichkeit, Konzentration, Lokalisation und Wechselwirkung von Molekülen punktgenau in biologischen Zellen bestimmen“, sagt Milton Stubbs. Es funktioniert also wie ein Hightech-Bewegungsmelder. Mit der neuen Apparatekombination will Bacia Wechselwirkungen von Proteinen und Lipid-Membranen charakterisieren. Auf diese Weise hofft sie zu verstehen, wie Proteine Membranen verformen und zum Beispiel sehr kleine kugelförmige Bläschen entstehen lassen können.