Wochenrückblick KW 46
Bayer, Roche und Qiagen bauen um
Die Pharma- und Biotech-Branche ist im Umbruch: Gleich mehrere Branchengrößen haben in den vergangenen Tagen groß angelegte Restrukturierungspläne bekanntgegeben.
Der Leverkusener Pharmakonzern Bayer wird weltweit 4.500 Stellen abbauen, allein in Deutschland sind es 1.700. Davon entfallen 700 Stellen auf den Bereich Healthcare und 300 Stellen auf die Sparte CropScience. In der Verwaltung und den zentralen Serviceeinheiten werden weitere 700 Stellen gestrichen. Ab 2013 sollen jährlich 800 Mio. Euro eingespart werden. Mit den frei werdenden Mitteln will der erst vor wenigen Wochen eingesetzte Vorstandsvorsitzende Marjin Dekkers vor allem die Pharma- und Pflanzenschutzsparte stärken. Außerdem soll die Präsenz in Schwellenländern ausgebaut werden, dort entstehen in den nächsten Jahren bis zu 2.000 neue Stellen.
Nicht nur in Leverkusen wird gespart, auch beim Schweizer Pharma- und Diagnostikspezialisten Roche stehen große Veränderungen an: „Roche steigt aus der RNAi-Technologie aus, alle Aktivitäten werden aufgegeben“ bestätigte Johannes Ritter, Kommunikationschef von Roche in Penzberg. Dementsprechend wird der Standort Kulmbach, das firmeneigene Exzellenzzentrum für RNA-Therapeutika, mit 70 Mitarbeitern geschlossen.
| Mehr auf biotechnologie.de |
biotechnologie.tv: 55. Folge - Millionenschwere Investition von Roche in Penzberg Wochenrückblick: Qiagen investiert 27 Millionen Euro |
Der Pharmakonzern hatte das Werk erst 2007 vom amerikanischen RNAi-Spezialisten Alnylam gekauft. Findet sich kein neuer Käufer, sollen spätestens im Juni 2011 die Lichter ausgehen. Die strategische Neuausrichtung ist Teil des Effizienzprogramms „Operational Excellence“, mit dem der Baseler Konzern jährlich bis zu 1,8 Mrd. Euro einsparen will. Andere Unternehmensteile in Deutschland sind von den Einschnitten aber nicht betroffen. Innerhalb des Effizienzprogramms wird die Diagnostics-Sparte in Penzberg die chemische Produktion und Analytik aus Mannheim übernehmen. Dort werden künftig die Diabetes Care-Aktivitäten gebündelt, die bisher für die Entwicklung von Insulinpumpen zuständige Niederlassung im Schweizer Burgdorf wird aufgegeben.
Mit der Qiagen N.V. hat auch Deutschlands größtes Biotech-Unternehmen Restrukturierungsmaßnahmen angekündigt. In der Hildener Zentrale werden die Aufgabenbereiche von 60 Mitarbeitern angepasst. Einige ohnehin frei werdende Stellen werden nicht neu besetzt, sieben Mitarbeitern wurde betriebsbedingt gekündigt. In Zukunft will Qiagen sich auf neue Vertriebsstrategien für seine molekulare Diagnostik konzentrieren. Das Unternehmen macht inzwischen die Hälfte seines Geschäfts auf dem Feld der molekularen Diagnostik. In diesem Bereich soll die Stellenzahl in der Zukunft sogar noch steigen. Mit der nun begonnenen Reorganisation sollen Umsatzrückgänge in den USA aufgefangen werden.
Mutation macht Schweinegrippe-Virus lebensbedrohlich
Der Austausch eines einzigen Proteinbausteins in der Hülle des Schweinegrippe-Virus bewirkt, dass der Erreger neue Zelltypen befällt und lebensbedrohliche Atemwegsbeschwerden auslösen kann.
Das haben Wissenschaftler aus Marburg und London herausgefunden. Die veränderten Influenza-Viren infizieren bevorzugt bewimperte Zellen in Lunge und Bronchien.
Die Forscher berichten in der Fachzeitschrift Journal of Virology (2010, Bd. 84 , S.12069) über ihre Ergebnisse. Die „Neue Grippe“ weitete sich im vergangenen Jahr zu einer weltweiten Seuche aus, verursacht durch das Influenzavirus H1N1; erst vor kurzem gab die Weltgesundheitsorganisation WHO Pandemie-Entwarnung. „Auch wenn die meisten Krankheitsfälle mild verliefen, verursachte das Virus mitunter schwere und sogar tödliche Infektionen“, resümieren die Autoren.
Um den Grund für die gravierende Krankheitsverläufe zu ermitteln, untersuchten die Wissenschaftler einige Virusvarianten genauer. Dazu analysierten sie Bestandteile des Oberflächenproteins Hämagglutinin genauer. Hämagglutinin ist dasjenige Virusprotein, das an Rezeptoren auf der Wirtszelle bindet; außerdem ist es daran beteiligt, dass Virushülle und Zellmembran miteinander verschmelzen, wodurch das Virusgenom ins Zellinnere gelangen kann.
| Mehr auf biotechnologie.de |
News: Schweinegrippe - Impfstoff für Deutschland kommt aus Dresden biotechnologie.tv: Folge 10 - Expertensicht zur Schweinegrippe News: RNA-Interferenz ermöglicht neue Strategie gegen Grippe |
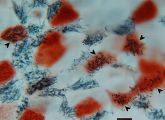
Die Autoren untersuchten Varianten des Grippeerregers, deren Hämagglutinin-Proteine an der Position D222G mutiert sind: Dort ist genau eine Aminosäure ausgetauscht. Wer sich mit dieser Virusvariante ansteckt, ist besonders stark gefährdet, schwer oder gar tödlich an Grippe zu erkranken. Wie die Forscher nachwiesen, infiziert das veränderte Virus in stärkerem Maße Zellen, die mit Flimmerhärchen oder Wimpern ausgestattet sind.
Solche Zellen kleiden unter anderem Lungen und Bronchien aus und verfügen vorwiegend über eine bestimmte Rezeptorvariante. „Es gibt einen klaren Zusammenhang zwischen der verbesserten Bindung an diesen Rezeptor und der vermehrten Infektion bewimperter Zellen“, so Mikhail Matrosovich vom Institut für Virologie der Philipps-Universität. Wenn die bewimperten Zellen der Atemwege befallen sind, ist der Organismus nicht mehr in der Lage, Schleim aus der Lunge zu transportieren und auf diese Weise Keime zu entfernen. „Die veränderte Rezeptorvorliebe und Umorientierung auf bewimperte Zellen kennzeichnen einen Krankheitserreger von erhöhter Gefährlichkeit“, schlussfolgern die Wissenschaftler; „dies unterstreicht die Notwendigkeit, die Evolution der Viren genau zu verfolgen“.
Neuer Typ von Immunzellen schützt vor Herzentzündungen
Biomediziner der Universität Rostock haben Immunzellen gefunden, die ein geschädigtes Herz vor übersteigerten Entzündungsreaktionen schützen helfen.
Demnach sorgen die neu entdeckten T-Lymphozyten im Blut dafür, dass die körpereigene Immunabwehr nach einem Herzinfarkt das betroffene Organ nicht noch zusätzlich angreift. Die Forscher vom Referenz- und Translationszentrum für kardiale Stammzelltherapie der Universität Rostock (RTC) berichten im Journal of Immunology (15. November 2010, Bd. 185, S.6286) über ihre Ergebnisse.
| Mehr auf biotechnologie.de |
News: Nach Herzinfarkt - Stammzelltherapie zeigt Wirkung News: Rostock eröffnet Zentrum für Stammzelltherapie im Herz |
Die Beschreibung des neuen Zelltyps erklärt nach Angaben der Forscher wichtige Zusammenhänge von Hormon- und Immunsystem und könnte die Entwicklung neuer Therapien für Herzkranke befeuern. Die Forscher um Jun Li waren bei Versuchen mit Ratten, die einen Herzinfarkt erlitten hatten, auf die sogenannten CD8+AT2R+T-Zellen gestoßen. Diese Immunzellen tragen bestimmte Rezeptoren auf ihrer Oberfläche, an die das Hormon Angiotensin II andocken kann. Auf diese Weise kontrolliert das Hormon den Blutdruck und den Wasserhaushalt des Körpers. Der neue Zelltyp der CD8+AT2R+T-Zellen ist eine Untergruppe von T-Lymphozyten, die auf die Erkennung ausgesuchter Antigene spezialisiert sind. Sieben Tage nach dem Infarkt fanden die Wissenschaftler eine signifikant erhöhte Zahl der Zellen im Herzen und in der Milz der Tiere.
Sie konnten auch die Funktion dieses Zelltyps ermitteln: die T-Lymphozyten fördern die Produktion eines speziellen Botenstoffs des Immunsystems namens IL-10, der seinerseits die Körperabwehr reguliert und damit vor übersteigerten Entzündungsprozessen schützt. Denn das Immunsystem des Menschen reagiert nicht immer angemessen auf eine Entzündung. „Oft schädigt eine übersteigerte Reaktion des Immunsystems die befallenen Organe mehr als nötig wäre, um den Angriff abzuwehren“, sagt Forscher Jun Li. Ein Beispiel dafür sei, dass in Folge eines Herzinfarktes oft große Areale des Herzmuskels absterben, vernarben und dann nicht mehr zur Herzfunktion beitragen könnten.
Die Rostocker Arbeitsgruppe denkt bereits über die Möglichkeit einer therapeutischen Anwendung des neu entdeckten Zelltyps nach. Durch gezieltes Verabreichen von CD8+AT2R+T-Zellen könnte die Immunreaktion des Körpers so weit gesteuert werden, dass nach einem Herzinfarkt die Rettung des geschädigten Herzmuskels wahrscheinlicher wird. Tatsächlich wurde bei Ratten durch Gabe von CD8+AT2R+ T-Zellen nach einem Herzinfarkt die Größe des Infarkts reduziert. Bis diese Therapie auf menschliche Patienten übertragen werden kann, sind jedoch noch mehrjährige Studien zu Sicherheit und Wirksamkeit nötig.
Organisiertes Zell-Gewimmel im Lymphknoten
Das auf den ersten Blick chaotische Hin und Her von tausenden Zellen in einem Lymphknoten folgt einem hochgeordneten System.
Das zeigen neue Rechenmodelle von Forschern des Helmholtz-Zentrums für Infektionsforschung (HZI) in Braunschweig und Forschern der Rockefeller University und der New York School of Medicine. Wie die Forscher im Fachjournal Cell (2010, Bd.143, S.592) berichten, durchlaufen Immunzellen beim Hin- und Herwandern im Lymphknoten einen Optimierungs-Zyklus, an dessen Ende die passende Immunantwort auf den jeweils eingedrungenen Erreger steht.
| Mehr auf biotechnologie.de |
News: Multiple Sklerose - Wie Immunzellen ins Gehirn eindringen |
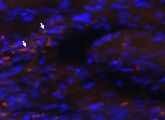
Immunzellen reifen im Lymphknoten in sogenannten Keimzentren heran. Diese werden räumlich in eine helle und eine dunkle Zone eingeteilt. Jedoch haben Wissenschaftler bis heute nicht vollständig verstanden, was in den beiden Zonen genau geschieht und welche Rolle die Bewegung der Abwehrzellen zwischen ihnen spielt. „Das scheinbare Chaos im Lymphknoten ist in Wirklichkeit hochgradig geordnet“, sagt Michael Meyer-Hermann, Leiter der HZI-Abteilung für System-Immunologie. Um den Weg einzelner Zellen im Lymphknoten zu verfolgen, entwickelten die US-amerikanischen Kooperationspartner eine neue Markierungs-Methode: Die Wissenschaftler hatten Mäuse gentechnisch verändert und dadurch die Immunzellen mit einem Farbstoff ausgestattet. Der Farbstoff leuchtet nur dann auf, wenn er mit Licht einer bestimmten Wellenlänge aktiviert wird.
Analysen und Berechnungen zeigten, dass der Informationsaustausch im Lymphknoten auf einer geordneten Bewegung der Zellen auf, die zwischen den beiden Zonen hin und her wandern. Dieser Prozess ist eine Art Castingshow: Runde für Runde werden nur die besten Abwehrzellen ausgewählt. Denn nur so können sie dem Organismus die optimalen Waffen, nämlich wirksame Antikörper, zur Verfügung zu stellen. „Es ist ein sich permanent wiederholender Zyklus von Veränderung in der dunklen Zone und Auswahl guter Zellen in der hellen Zone“, sagt Meyer-Hermann. „Die Immunzellen vermehren sich, mutieren und verändern dabei ihre Antikörper leicht. Das Immunsystem wählt dann die besten Zellen aus. Dann beginnt der Zyklus von neuem. Am Ende steht die Produktion von optimierten Antikörpern.“Die neuen Erkenntnisse zur Auswahl von Immunzellen und Optimierung einer Immunantwort können laut Michael Meyer-Hermann entscheidend dabei helfen, in Zukunft Impfungen zu verbessern. Denn auch hier spiele die Bildung hoch wirksamer Antikörper im Körper eine wichtige Rolle, so der Wissenschaftler.
Fünf neue biologische DFG-Sonderforschungsbereiche
Die Deutsche Forschungsgemeinschaft (DFG) richtet zum 1. Januar 2011 elf neue Sonderforschungsbereiche (SFB) ein. Fünf von ihnen beschäftigen sich mit molekularbiologischen Themen. Wie der zuständige Bewilligungsausschuss auf seiner Herbstsitzung in Bonn beschloss, werden die neuen SFB mit insgesamt 94,4 Millionen Euro zunächst für eine erste Förderperiode von vier Jahren gefördert.
- SFB 889 „Zelluläre Mechanismen sensorischer Verarbeitung“
Der SFB 889 will die die Funktion sensorischer neuronaler Netzwerke bei der Sinneswahrnehmung untersuchen. Dabei werden verschiedene Spezies – Fliegen, Mäuse, Primaten – und Sinnesmodalitäten – Sehen, Hören, Riechen, Fühlen – betrachtet.
Leitung: Universität Göttingen - SFB 937 „Kollektives Verhalten von weicher und biologischer Materie“
Insgesamt will der SFB zum besseren Verständnis der Phänomene in Polymernetzwerken und Biomembranen beitragen – eine wichtige Voraussetzung, um die komplexe Organisation und Dynamik zellulärer Einheiten beschreiben zu können.
Leitung: Universität Göttingen - SFB 938 „Milieuspezifische Kontrolle immunologischer Reaktivität“
In ihm geht es um die molekulare Analyse immunologischer Prozesse in verschiedenen Geweben und Organen vor allem des Menschen sowie weiterer Modellorganismen.
Leitung: Universität Heidelberg - SFB 944 „Physiologie und Dynamik zellulärer Mikrokompartimente"
Der SFB erweitert den Begriff der Mikrompartimente und bezeichnet damit funktionelle Untereinheiten innerhalb der Zelle. Die Forscherinnen und Forscher richten ihren Blick auf die Funktion, Regulation und dynamische Zusammensetzung von ausgewählten Mikrokompartimenten, um Grundprinzipien ihrer Funktionsweise abzuleiten.
Leitung: Universität Osnabrück - SFB 894 „Ca2+-Signale: Molekulare Mechanismen und Integrative Funktionen“
Calciumionen gehören zu den wichtigsten Signalmolekülen. Die Forscher wollen die Bedeutung subzellulärer Calciumionen+-Signale in Zellen klären. Im Einzelnen sollen die Entstehung und der Verlauf elementarer Ca2+-Signale in Zellen des Immunsystems, des zentralen Nervensystems, des Herz-Kreislauf-Systems, des sensorischen Systems und des neuroendokrinen Systems untersucht werden.
Universität des Saarlandes
Zur ausführlichen Beschreibung der neuen Sonderforschungsbereiche auf dfg.de: hier klicken
Stammzellforschung: 12 Millionen Euro für Projekte mit US-Instituten
Dank einer Millionenförderung werden drei deutsche Wissenschaftlerteams künftig gemeinsam mit Kollegen in Kalifornien Projekte in der Stammzellforschung vorantreiben.
Das Bundesministerium für Bildung und Forschung (BMBF) unterstützt die deutsch-amerikanische Kooperation mit insgesamt bis zu 12 Millionen Euro. Die drei deutschen Forschergruppen sind damit die ersten, die sich erfolgreich bei den Ausschreibungen des kalifornischen Instituts für Regenerative Medizin (CIRM) beteiligt haben. Das kalifornische CIRM ist die weltweit bedeutendste Forschungsfördereinrichtung auf dem Gebiet der Stammzellforschung.
| Mehr auf biotechnologie.de |
News: Deutsch-amerikanische Kooperation - Dritte Runde mit Fokus Stammzellen gestartet Wochenrückblick: Deutsch-amerikanische Förderinitiative in der Regenerativen Medizin gestartet |
Im Rahmen von deutsch-amerikanischen Projekten sollen vielversprechende Ergebnisse der grundlegenden Stammzellforschung für eine medizinische Anwendung weiterentwickelt werden. "Gerade in einem so dynamischen Forschungsfeld wie der Stammzellforschung ist der internationale Austausch von entscheidender Bedeutung, damit wissenschaftlicher Fortschritt gelingt und die Forschungsergebnisse schnell in den Markt kommen", sagte Bundesforschungsministerin Annette Schavan anlässlich der Auswahl der ersten deutsch-amerikanischen Projektteams. "Wir müssen weltweit die besten Forscherinnen und Forscher zusammenbringen, damit die Therapie mit Stammzellen nicht länger nur Wunschdenken bleibt", so Schavan.
Die drei ersten Teams im Überblick:
- Ein Team um Oliver Brüstle von der Universität Bonn will eine stammzellbasierte Therapie für Patienten mit der neurodegenerativen Erkrankung Canavan entwickeln. Die körpereigenen Stammzellen sollen dabei so umprogrammiert werden, dass sie die Funktion eines Gens wiederherstellen, das als Ursache für die Erkrankung gilt.
- Um die Behandlung von Wunden bei Diabetes-Erkrankungen geht es in einem Projekt, an dem José Tomás Egana von der TU München beteiligt ist. Zusammen mit kalifornischen Kollegen sollen künstliche Gewebeersatzstrukturen mit körpereigenen Stammzellen besiedelt werden. Dies, so die Hoffnung, könnte die Wundheilung bei Diabetes-Patienten beschleunigen.
- Sogenannte Krebsstammzellen haben die Wissenschaftler um Andreas Hochhaus vom Universitätsklinikum Jena im Blick. Diese speziellen Stammzellen werden dafür verantwortlich gemacht, dass Krebsgeschwüre oftmals wiederkehren und sich durch eine Therapie nicht komplett entfernen lassen. Gemeinsam mit kalifornischen Wissenschaftlern sollen die besonderen Resistenzeigenschaften von Krebsstammzellen gegenüber Krebsmedikamenten untersucht werden, um dadurch effektivere Therapien zu ermöglichen.