Aufgeblasene Eiweiße wirken länger
-
 <ic:message key='Bild vergrößern' />
<ic:message key='Bild vergrößern' />
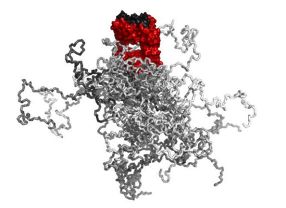
- Ein Antikörperfragment (rot-schwarz) erhält durch eine lange Aminosäurekette, die aus Prolin, Alanin und Serin (PAS) besteht, eine Art "Ballon", der die Halbwertszeit im Blut verlängert. Quelle: Arne Skerra / TUM
23.09.2009 -
Wer an chronischer Hepatitis B leidet, wird mit dem Botenhormon Interferon behandelt. Das Problem: Interferon ist ein sehr kleines Eiweiß, weshalb es bereits nach kurzer Zeit wieder über die Niere ausgeschieden wird. Damit die Wirkung nicht nachlässt, brauchen die Patienten alle zwei Tage eine hoch dosierte Spritze. Wissenschaftlern um Arne Skerra von der Technischen Universität München ist es gelungen, kleine Eiweiße mit einer Art molekularem Ballon zu verbinden, der sich aufbläht und dadurch die Halbwertszeit der Proteine im Körper verlängert. Aufbauend auf ihren Ergebnissen haben die Forscher nun die XL-protein GmbH gegründet.
Viele Biopharmazeutika bestehen aus kleinen Eiweißen, die rasch wieder aus dem Körper ausgeschieden werden. So werden bei der chronischen Form der Hepatitis B zum Beispiel Interferone verabreicht. Interferone wurden 1957 als zelluläre Abwehrstoffe gegen die Ausbreitung von Virusinfektionen im Gewebe entdeckt. Sie wirken als Alarm fürs Immunsystem und aktivieren die T-Abwehrzellen, die virusbefallene oder durch Krebs entartete Zellen angreifen. Ein Problem der Interferone ist aber ihre kurze Verweildauer im Körper. Werden Sie ins Blut gespritzt, beginnt die Niere unverzüglich damit, sie auszufiltern. Deshalb mussten Patienten früher alle zwei Tage eine hoch dosierte Spritze verabreicht bekommen, um den Nachschub an Interferonen aufrechtzuerhalten.
| Mehr zum Thema auf biotechnologie.de |
Wochenrückblick: Wirkstoff aus Tränen als Werkzeug für Krebstherapie News: BioBrowser: Kleine Eiweiße ganz groß |
Von der PEGylierung zur PASylierung
Deutlich länger bleibt Interferon dagegen im Körper, wenn es chemisch mit einem synthetischen PEG-Molekül (Polyethylenglycol) gekoppelt ist. PEG ist eine Art Knäuel aus einem langkettigen Polymerfaden, das Wasser aufsaugt und sich dadurch aufbläht. Auf diese Weise wird das PEG-Molekül so groß, dass es nicht durch die feinen Poren der Niere passt - das angekoppelte Interferon wird daher länger im Blutkreislauf gehalten, und der Patient muss nur eine Spritze alle ein bis zwei Wochen erhalten. Bei Interferon ist die Technik schon seit längerem etabliert. Im Mai 2000 wurde das erste "pegylierte" Interferon auf dem europäischen Markt zugelassen. Essex Pharma, eine Tochter des US-Konzerns Schering-Plough, vertrieb es unter dem Handelsnamen "PegIntron" (Interferon α-2b). 2002 brachte der Schweizer Pharmakonzern Roche die Weiterentwicklung des seit 1987 erhältlichen Interferon α-2a unter dem Handelsnamen "Pegasys" auf den Markt. Beide Medikamente wirken gegen Hepatitis-C, Pegasys seit 2007 auch gegen Hepatitis-B.
Wissenschaftler der Technischen Universität München (TUM) versuchen nun, die Wirkung von PEG zu erhalten, ohne die damit verbundenen Nachteile in Kauf nehmen zu müssen. Die Forscher um Arne Skerra vom Lehrstuhl für Biologische Chemie am Wissenschaftszentrum Weihenstephan haben mit biotechnologischen Methoden einen Aminosäurefaden entwickelt, der sich ähnlich wie PEG verknäult und Wasser anlagert. Im Gegensatz zu vielen PEG-Verbindungen besteht jedoch nicht die Gefahr, dass sich dieses Anhängsel im Körper anreichert. Vielmehr wird es - über einen längeren Zeitraum - ausgeschieden oder biologisch abgebaut. Denn der Aminosäurefaden ist aus lediglich drei der 20 natürlich vorkommenden Aminosäuren zusammengesetzt: Prolin, Alanin und Serin, kurz PAS. Die wenig komplexe Verbindung macht dem Körper beim Recycling keine Probleme.
| XL-protein GmbH |
Im Frühjahr gründeten die Wissenschaftler der Technischen Universität München das Start-Up, um ihre PAS-Technologie zu vermarkten. Das Unternehmen hat seinen Sitz in Freising bei München. zur Firmenwebsite: hier klicken |
Wirkstoffe belieben bis zu 60-mal länger im Blut
Die Kombination des PAS-Anhängsels mit Interferon schlägt die herkömmliche PEG-Technik offenbar auch in der Wirksamkeit. In ersten Versuchen mit Tieren stellten die Münchener Wissenschaftler fest, dass ein PASyliertes Interferon eine um den Faktor 60 verlängerte Halbwertszeit im Blut aufweist, so dass damit tatsächlich verlängerte Dosierungsintervalle ermöglicht werden. Ein weiterer Vorteil liegt in der vereinfachten biotechnologischen Herstellung, denn die DNA-Stücke, die die Informationen für den PAS-Aminosäurefaden beziehungsweise das Interferon tragen, werden einfach aneinandergehängt und dann zum Beispiel in ein Bakterium eingepflanzt. Das Bakterium produziert das PASylierte Interferon gleichsam am Stück, so dass anders als bei einer chemischen Kopplung von PEG mit Interferon wesentlich weniger Herstellungsschritte nötig sind.
"Dadurch werden die Produktionskosten erheblich sinken", vermutet Skerra. Mit einem PAS-Anhängsel versehen lassen sich prinzipiell alle kleinen Eiweiße, die bereits als Medikamente eingesetzt oder bei Pharmafirmen derzeit entwickelt werden, wie zum Beispiel Wachstumsfaktoren oder funktionelle Antikörperfragmente. Ein großer Markt. Um die Entdeckung auch wirtschaftlich zu nutzen, hat Skerra deshalb zusammen mit seinen Mitarbeitern die Biotech-Firma XL-protein GmbH gegründet, die im Frühjahr 2009 ihre Geschäftstätigkeit aufgenommen hat. "Unsere Technologie hat das Potenzial dazu, Blockbuster-Medikamente einer neuen Generation hervorzubringen", davon ist Biochemiker Skerra überzeugt. Mehrere der neuen Wirkstoffe seien bereits im Stadium der fortgeschrittenen präklinischen Entwicklung.
In der Biotech-Szene ist Skerra längst kein Neuling mehr. Er war maßgeblich an der Entwicklung der Antikörper-Technologie beteiligt, auf der das Unternehmen MorphoSys aufbaut. Skerra ist zudem einer der Gründer der Firma Pieris, die bestimmte Eiwieße, sogenannte Lipocaline, unter anderem bei der Krebsbehandlung einsetzen will (mehr...).